Enseignement scientifique première
Durée 1h – 10 points – Thème « Une longue histoire de la matière »
[latexpage]
L’argent est connu depuis des millénaires et son utilisation pour des applications industrielles s’est fortement développée au XXème siècle.
L’argent est l’élément chimique de numéro atomique Z = 47 et de symbole Ag. À l’état métallique, il est blanc, très brillant, malléable ainsi que très ductile (c’est-à-dire qu’il peut être étiré sans se rompre).
Données :
Nombre d’entités par mole : N = 6,022×1023 mol-1.
Rayon moyen d’un atome d’argent : r = 1,45 Å. L’angström (Å) est une unité de longueur utilisée en cristallographie valant 10-10 m.
Document 1. Maille élémentaire du cristal d’argent
À l’état microscopique, l’argent métallique solide est organisé selon un réseau cubique à faces centrées.
Figure 1a : représentation en perspective cavalière
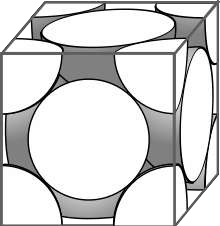
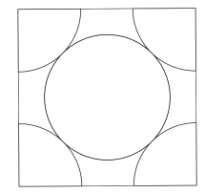
Figure 1b : vue de l’une des faces du cube
Document 2. Les minerais d’argent
L’argent est rarement présent dans le sous-sol à l’état natif (pépite ou filon). Cependant dans les minerais, on le trouve souvent associé à d’autres éléments chimiques : par exemple, dans la chlorargyrite de formule AgCl, il est associé à l’élément chlore Cl ; dans l’acanthite de formule Ag2S, il est associé à l’élément soufre S.
Figure 2a : maille élémentaire de la chlorargyrite
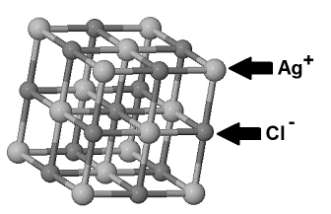
Cl– : ion chlorure
Figure 2b : maille élémentaire de l’acanthite
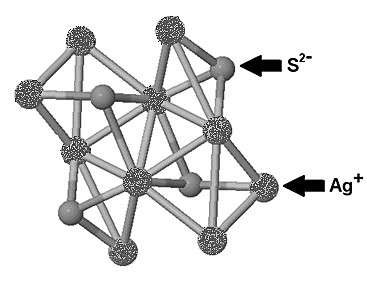
S2- : ion sulfure
Document 3. Analyse d’un échantillon du gisement minier d’Ain-Kerma
Le gisement minier d’Ain-Kerma est situé en Algérie à 15 km au Nord-Ouest de la ville de Constantine. Il a été activement exploité de 1913 à 1951 pour son minerai contenant 40 % d’antimoine de symbole chimique Sb.
Figure 3 : Échantillon de minerai observé au microscope électronique
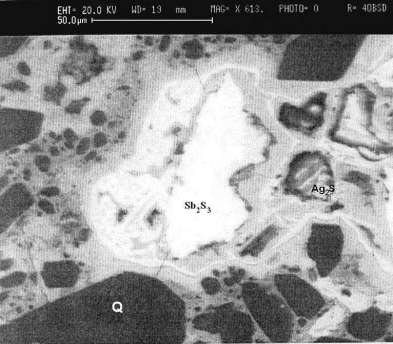
Quartz (Q)
Acanthite (Ag2S)
D’après https://www.researchgate.net/publication/279533102_Testing_of_Silver_Sulphide_in_Antimony_Mineralization_Hydrothermal_Karst_Formations_Ain-Kerma
1 – En utilisant la figure 1a, montrer en explicitant la démarche que le nombre d’atomes contenus dans une maille élémentaire du cristal d’argent est égal à 4.
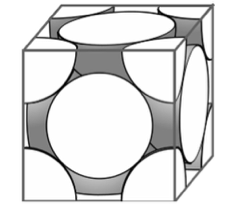
Il y a 8 atomes sur les sommets qui sont dans 1/8 de la maille.
Il y a 6 atomes sur les faces qui sont dans 1/2 de la maille.
N=8×1/8+6×1/2=4
Il y a 4 atomes dans une maille.
2- En utilisant la figure 1b et en notant 𝑎 le paramètre de maille du cristal d’argent (égal à la longueur de l’arête du cube), démontrer que √2 a=4r . En déduire que 𝑎 = 4,10 Å.
D’après le théorème de Pythagore :
\[\left(4r\right)^2=a^2+a^2\]
\[16r^2=2a^2\]
\[\sqrt{2a^2}=\sqrt{16r^2}\]
\[\sqrt{2}a=4r\]
\[a=\frac{4r}{\sqrt{2}}\]
\[a=\frac{4\times 1,45}{\sqrt{2}}\]
𝑎 = 4,10 Å
3 – Calculer la compacité du cristal d’argent et en déduire que 26 % de la maille élémentaire est vide. On rappelle que la compacité d’un cristal est égale au rapport du volume des atomes contenus dans une maille élémentaire par le volume de cette maille.
\[C=\frac{\textrm{Volume occupé par les atomes d’une maille}}{\textrm{Volume de la maille}} \]
\[\textrm{Volume occupé par les atomes d’une maille}=a^3 \]
Chaque atome au sommet du cube appartient à huit mailles et ceux au centre de chaque face appartiennent à deux mailles :
N=8×1/8+6×1/2=4
Volume occupé par les atomes d’une maille=N×V0
Avec :
\[V_0=\frac{4}{3}\pi r^3\]
\[C=\frac{N \times V_0}{a^3} \]
\[C=\frac{4 \times\frac{4}{3}\pi r^3}{a^3} \]
Or
\[r =\frac{a\sqrt{2}}{4} \]
\[C=\frac{4 \times\frac{4}{3}\pi (\frac{a\sqrt{2}}{4})^3}{a^3} \]
\[C=\frac{4 \times\frac{4}{3}\pi (\frac{a^3\sqrt{2}^3}{4^3})}{a^3} \]
\[C=4 \times\frac{4}{3}\pi \times \frac{\sqrt{2}^3}{4^3} \]
C=0,74
Les atomes occupent donc 74% de l’espace d’une maille.
Calculons l’espace vide : 100-74=26%
On déduit donc que 26 % de la maille élémentaire est vide
4 – La masse volumique de l’argent sous forme cristalline vaut approximativement 10,5×103 kg∙m-3. Calculer la masse d’un atome d’argent après avoir déterminé le volume d’une maille du cristal.
\[\rho=\frac{m_{maille}}{V_{maille}} \]
Or
\[m_{maille}=N\times m \]
\[V_{maille}=a^3 \]
\[\rho=\frac{N\times m}{a^3} \]
\[\frac{N\times m}{a^3}=\rho \]
\[m =\frac{\rho\times a^3}{N} \]
\[m =\frac{10,5.10^3\times (4,10.10^{-10})^3}{4} \]
\[m =1,81.10^{-25} kg \]
5 – La chlorargyrite et l’acanthite sont des cristaux. Préciser le sens du mot cristal et donner un exemple d’un autre mode d’organisation de la matière solide à l’échelle microscopique.
Les cristaux sont des édifices chimiques possédant une structure en trois dimensions parfaitement ordonnée.
Un exemple d’un autre mode d’organisation de la matière solide à l’échelle microscopique : un solide amorphe comme le verre.
6 – Expliquer pourquoi le minerai d’Ain-Kerma peut être qualifié de roche et pourquoi cette roche peut être qualifiée d’argentifère.
Une roche est formée de l’association de cristaux d’un même minéral ou de plusieurs minéraux.
Le minerai d’Ain-Kerma contient les minéraux suivants :
- Stibine (Sb2S3)
- Quartz (Q)
- Acanthite (Ag2S)

Le minerai d’Ain-Kerma peut donc être qualifié de roche.
Le minerai d’Ain-Kerma contient de l’Acanthite de formule (Ag2S). Il contient de l’argent. Le minerai d’Ain-Kerma peut donc être qualifiée d’argentifère.
