E3C2 – 10 points – Durée 1h – calculatrice autorisée
Sujet n°G1SPHCH02796
Télécharger l’exercice en PDF :
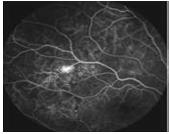
L’angiographie est une analyse médicale qui consiste à photographier les artères et les veines afin de déceler éventuellement des anomalies circulatoires telles que des lésions, des anévrismes, etc. Dans le cas particulier de l’angiographie rétinienne on injecte un colorant fluorescent tel que la fluorescéine au patient. Ce colorant est transporté dans tout le réseau artériel et veineux de la rétine. Des clichés sont pris au cours du temps et leur analyse permet d’établir le diagnostic. L’image ci-dessous est l’image obtenue suite à une angiographie rétinienne d’un patient diabétique. Elle révèle une rétinopathie qui se caractérise par l’existence d’une tâche blanche sur la rétine.
Les objectifs de cet exercice sont les suivants :
- comprendre l’origine physique du phénomène de fluorescence en étudiant l’expérience de Stokes ;
- l’étude du principe de photographie réalisée lors de l’angiographie ;
- l’analyse d’une solution de fluorescéine.
I. Origine physique du phénomène de fluorescence
Les travaux de nombreux scientifiques ont contribué à la compréhension de l’origine de la fluorescence ainsi qu’à son utilisation au quotidien dans la détection, les analyses et les diagnostics. Parmi ces scientifiques nous pouvons citer Sir Gabriel Stokes (1819-1903) dont l’expérience est décrite ci-dessous.
En 1852, Sir Georges Gabriel Stokes, professeur de mathématiques et de physique à l’université de Cambridge étudia les propriétés d’une solution de sulfate de quinine dont la surface est de couleur bleue lorsqu’elle est éclairée en lumière blanche…
L’expérience qu’il réalise consiste, dans un premier temps, à décomposer la lumière du Soleil par un prisme afin d’obtenir un spectre d’émission. Puis il éclaire la solution de sulfate de quinine avec les différentes parties du spectre obtenu en allant du rouge au violet. Il observe que la solution est traversée par la quasi-totalité de la lumière qu’elle reçoit, sans perturbation particulière, lorsque les radiations se situent entre le rouge et bleu du spectre. Par contre lorsque la solution est éclairée avec les rayonnements violets du spectre visible et au-delà c’est-à-dire dans l’ultraviolet, la solution émet une lumière de couleur bleue.
Cette dernière observation permet à Sir Stokes de prouver que l’émission bleutée observée provient d’une absorption de la lumière dans l’ultraviolet. Il aboutit à la conclusion selon laquelle : « la longueur d’onde d’une lumière émise par une solution colorée sera supérieure à celle du rayonnement incident à l’origine de cette émission » : c’est la loi de Stokes.
Texte Inspiré de « Lumière et Phosphorescence » de Bernard Valeur
Données :
- Constante de Planck : h = 6,63×10–34 J.s ;
- 1 eV = 1,602×10–19 J ;
- la relation de Planck Einstein reliant ΔE, h, c et λ est supposée connue.
- Diagramme simplifié de Perrin-Jablonski
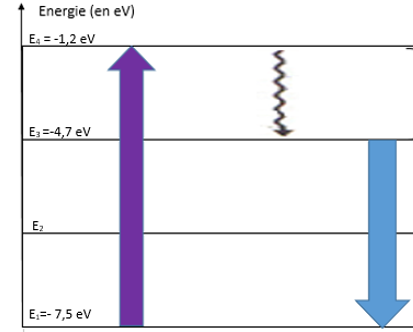
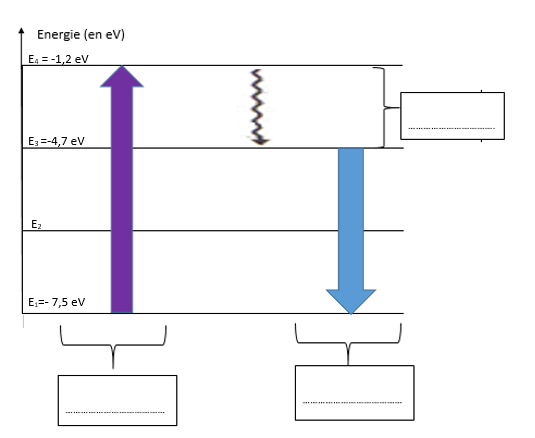
Le diagramme ci-contre est une représentation simplifiée de la voie de désexcitation d’une molécule fluorescente après absorption d’un photon du niveau fondamental au deuxième niveau d’énergie électronique.
La désexcitation comporte deux phases :
– la première qui porte le nom de processus de conversion interne permet à la molécule de passer d’un niveau excité supérieur à un niveau excité intermédiaire inférieur. Au cours de cette étape il n’y a pas d’émission de photons mais il peut y avoir des transferts thermiques.
– la deuxième phase, la fluorescence, est le retour à l’état fondamental avec émission d’un photon.
1. D’après les conclusions de Sir Gabriel Stokes, quelle est l’origine de la couleur bleue fluorescente de la solution de quinine ?
D’après les conclusions de Sir Gabriel Stokes, l’absorption de la lumière dans l’ultraviolet est l’origine de la couleur bleue fluorescente de la solution de quinine.
2. À partir des mots soulignés dans le document présentant le diagramme simplifié de Perrin-Jablonski, compléter l’annexe à rendre avec la copie.
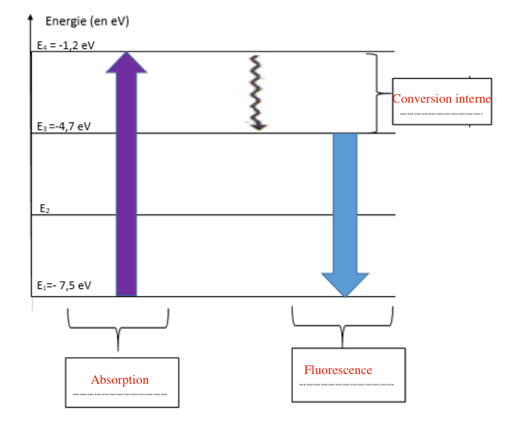
3. Proposer une explication, s’appuyant sur des calculs, permettant de justifier que les transitions représentées dans le diagramme simplifié de Perrin-Jablonski sont en accord avec la « loi de Stokes ».
$$\Delta E=h\times\nu=h\times\frac{c}{\lambda}$$
$$\lambda=\frac{h\times c}{|\Delta E|}$$
Pour l’absorption :
$$\lambda=\frac{6,63.10^{-34}\times(3,00.10^8)}{|(-1,2-(-7,5))\times1,602.10^{-19}|}=1,97.10^{-7}\ m=197\ nm$$
Pour la fluorescence :
$$\lambda=\frac{6,63.10^{-34}\times(3,00.10^8)}{|(-7,5-(-4,7))\times1,602.10^{-19}|}=4,43.10^{-7}\ m=443\ nm$$
L’absorption est donc bien dans l’ultraviolet et la solution émet une lumière de couleur bleue.
Les transitions représentées dans le diagramme simplifié de Perrin-Jablonski sont en accord avec la « loi de Stokes ».
II. Principes de la photographie réalisée lors de l’angiographie rétinienne
L’appareil photographique utilisé pour l’angiographie peut être modélisé par :
- une lentille convergente de centre O, correspondant à l’objectif. Sa distance focale image est égale à $\overline{OF’}$= f’ = 60 mm ;
- un écran correspondant au capteur numérique de l’appareil photographique.
On suppose par la suite que l’objectif de l’appareil photographique est proche de l’œil au cours de cette analyse médicale comme le montre le schéma ci-dessous.
Schéma représentant l’expérience réalisé, sans souci d’échelle.
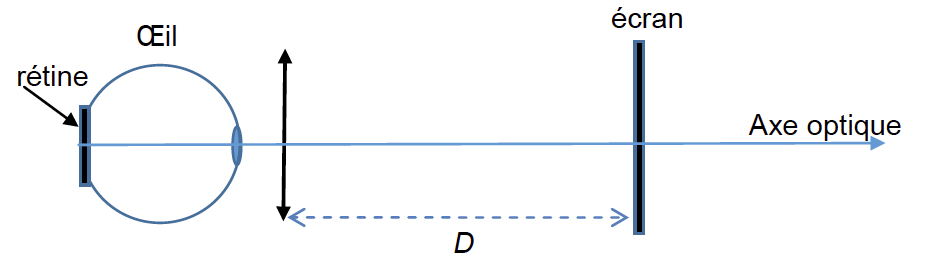
4. La tâche blanche présente sur la rétine est représentée par le segment AB. Son image sur l’écran est notée A’B’. Sachant que le grandissement de l’objectif de l’appareil photographique utilisé lors de cette analyse est $\gamma=\frac{\overline{OA’}}{\overline{OA}}=\frac{\overline{A’B’}}{\overline{AB}}$= -1, donner les caractéristiques de l’image de la tâche blanche formée sur le capteur numérique dans l’hypothèse où ɣ> 0.
$$ \frac{\overline{AB’}}{\overline{AB}}=-1$$
$$\overline{A’B’}=-\overline{AB}$$
$$A’B’=AB$$ donc l’image est de même taille que l’objet
$\overline{AB}>0$ et donc $\overline{A’B’}<0$ donc l’image est renversée
$$ \frac{\overline{OA’}}{\overline{OA}}=-1$$
$$\overline{OA’}=-\overline{OA}$$
Or $\overline{OA}<0$ , $\overline{OA’}>0$ donc l’image est réelle.
5. Exprimer, en fonction de f ‘ et ɣ , la distance $\overline{OA’}$ pour laquelle l’image de la tâche blanche est nette sur le capteur de l’appareil photographique. Donner la valeur de la distance D et commenter la valeur obtenue.
D’après la relation de grandissement :
$$\gamma=\frac{\overline{OA’}}{\overline{OA}}$$
$$\overline{OA}=\frac{\overline{OA’}}{\gamma}$$
D’après la relation de conjugaison :
$$\frac{1}{\overline{OA’}}-\frac{1}{\overline{OA}}=\frac{1}{f’}$$
$$\frac{1}{\overline{OA’}}-\frac{1}{(\overline{OA’}/\gamma)}=\frac{1}{f’}$$
$$\frac{1}{\overline{OA’}}-\frac{\gamma}{\overline{OA’}}=\frac{1}{f’}$$
$$\frac{1}{\overline{OA’}}(1-\gamma)=\frac{1}{f’}$$
$$\frac{1}{\overline{OA’}}=\frac{1}{f'(1-\gamma)}$$
$$\overline{OA’}=f'(1-\gamma)$$
$$\overline{OA’}=60.10^{-3}(1-(-1))=1,2.10^{-1}\ m$$
D’après la figure $D=OA’$
Donc $D=1,2.10^{-1}\ m$ soit $12\ cm$
La valeur obtenue parait cohérente avec la taille d’un appareil de mesure
III. Analyse de la solution de fluorescéine utilisée pour l’angiographie
La solution de fluorescéine utilisée lors de l’angiographie rétinienne doit avoir les caractéristiques suivantes :
- pour 100 mL de solution injectable ;
- une ampoule de 5 mL contient 0,5 g de fluorescéine sodique.
http://agence-prd.ansm.sante.fr/php/ecodex/rcp/R0287916.htm
On souhaite vérifier la concentration en fluorescéine d’une solution commerciale afin de s’assurer qu’elle puisse être utilisée lors d’une angiographie rétinienne.
Données :
- Formule brute de la fluorescéine : C20H1205 ;
- Masses molaires atomiques :
M(C) = 12,0 g.mol-1 ; M(H) = 1,0 g.mol-1 ; M(O) = 16,0 g.mol-1
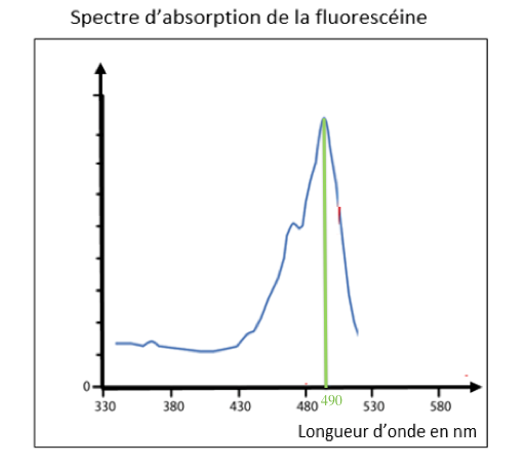
- Spectres d’absorption et de fluorescence de la fluorescéine :
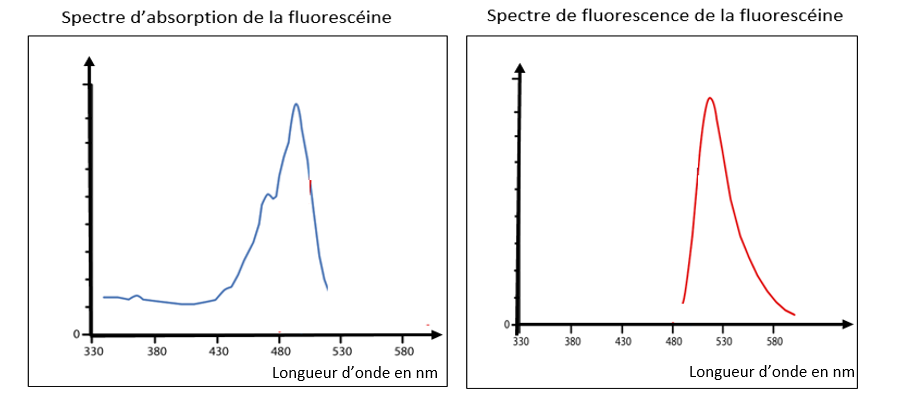
6. Les spectres d’absorption et de fluorescence de la fluorescéine sont- ils en accords avec la loi de Stokes ? Justifier votre réponse.
La loi de Stokes :
« la longueur d’onde d’une lumière émise par une solution colorée sera supérieure à celle du rayonnement incident à l’origine de cette émission »
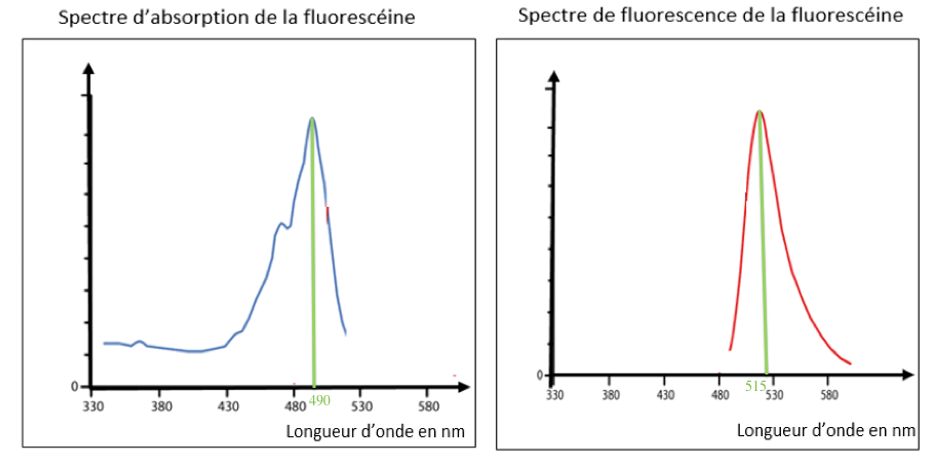
Ici, la longueur d’onde d’une lumière émise par une solution colorée $\lambda=515\ nm$ est supérieure à celle du rayonnement incident à l’origine de cette émission $\lambda=490\ nm$.
C’est en accord avec la loi de Stokes.
Pour déterminer la concentration en quantité de matière en fluorescéine de la solution commerciale, l’absorbance de plusieurs solutions de fluorescéine de concentrations en quantité de matière connues a été mesurée.
Les mesures ont permis d’obtenir les résultats suivants :
| Concentration C de la solution en µmol. L-1 | 1,5 | 3,0 | 4,5 | 6,0 | 7,5 | 9,0 |
| Absorbance A de la solution | 0,10 | 0,21 | 0,31 | 0,64 | 0,80 | 0,96 |
La courbe d’étalonnage représentant l’évolution de l’absorbance en fonction de la concentration en quantité de matière en fluorescéine est reproduite ci-dessous.
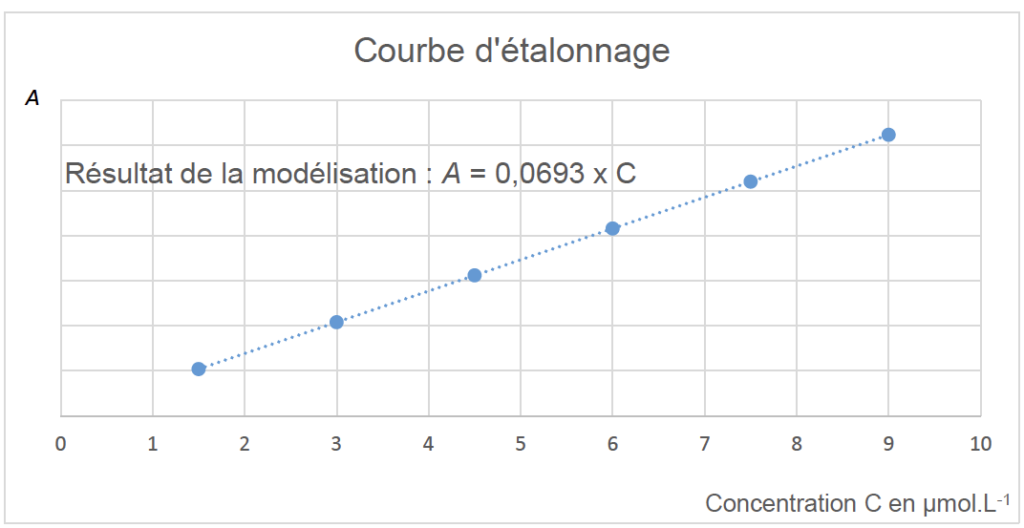
7. À quelle longueur d’onde doit-on se placer afin de réaliser les mesures décrites ? Justifier votre réponse.
On se place au maximum d’absorption soit à λmax=490nm.
Afin d’analyser la solution commerciale, il faut la diluer. On prépare ainsi une solution S1 en diluant 30 000 fois la solution commerciale.
8. La valeur de l’absorbance de la solution S1 mesurée étant de 0,67, déterminer la concentration en quantité de matière C de fluorescéine, contenue dans la solution commerciale.
On se place au maximum d’absorption soit à $\lambda_{max}=490\ nm$.
D’après le résultat de la modélisation : $A=0,0693\times C$
$$C=\frac{A}{0,0693}$$
Donc
$$C_{S_1}=0,67/0,0693=9,7\ \mu mol.L^{-1}$$
Or la solution $S_1$ a été obtenue en diluant $30\ 000$ fois la solution commerciale.
$$C=30\ 000\times C_{S_1}$$
$$C=30\ 000\times9,7.10^{-6}=0,29\ mol.L^{-1}$$
9. L’incertitude-type sur la valeur de C est estimée à ∆C = 0,02 mol.L-1 dans les conditions de l’expérience. Comparer la valeur expérimentale obtenue à la valeur retenue pour les angiographies rétiniennes. Conclure.
$$C_{exp}=0,29\pm0,02\ mol.L^{-1}$$
$$0,29-0,02<C_{exp}<0,29+0,02$$
$$0,27\ mol.L^{-1}<C_{exp}<0,31\ mol.L^{-1}$$
Calculons la valeur retenue pour les angiographies rétiniennes.
D’après l’énoncé : la fluorescéine ($C_{20}H_{12}O_5$) sodique : 10,00 g pour 100 mL de solution injectable
$$C=\frac{n}{V}$$
Or
$$n=\frac{m}{M}$$
d’ou
$$C=\frac{m}{M\times V}$$
$$C=\frac{10,00}{(20\times12,0+12\times1,0+5\times16,0)\times100.10^{-3}}=0,30\ mol.L^{-1}$$
Les deux valeurs sont en accord.
Annexe à rendre avec la copie