Sujet sans enseignement de mathématiques spécifique
Enseignement scientifique première
Durée 1h – 10 points – Thème « Une longue histoire de la matière »
Sujets n°ENSSCI1107 et n°ENSSCI1138
Télécharger l’exercice en PDF :
Des techniques de datation sur des objets géologiques ont permis de construire un modèle de l’évolution de la composition de l’atmosphère depuis la formation de la Terre. En étudiant quelques données sur l’uranium, on cherche à vérifier la validité d’une partie de ce modèle.
Document 1 – Fabriqué dans les étoiles
Il n’existe aucun noyau stable dont le numéro atomique serait supérieur à celui du bismuth (numéro atomique : 83). Pourtant, on trouve sur Terre des éléments plus lourds encore : le thorium et l’uranium. Ils sont radioactifs et ils ont été formés, au sein des étoiles, il y a plusieurs milliards d’années. […]
Dans une supernova, c’est-à-dire une étoile super massive qui s’effondre sur elle- même en quelques millisecondes, la densité de matière extrême permet à un noyau de capturer plusieurs neutrons en une seule fois. Le noyau subit ensuite plusieurs transformations radioactives successives qui génèrent des éléments beaucoup plus lourds, dont l’uranium. Puis, dans un rebond explosif, la supernova explose et expulse ces noyaux dans le milieu interstellaire. Ils peuvent ensuite se rassembler autour d’une nouvelle étoile et s’agréger pour se retrouver dans les planètes comme notre Terre.
Source : https://www.cea.fr/comprendre/Pages/radioactivite/essentiel-sur-uranium.aspx
1 – À l’aide du document 1 et de vos connaissances, déterminer le type de transformation nucléaire auquel appartient la formation de l’uranium au cœur des étoiles. Justifier votre réponse.
La formation de l’uranium au cœur des étoiles se fait par transformations nucléaires qui implique une réaction dans laquelle le noyau capture plusieurs neutrons puis des transformations radioactives successives qui génèrent des éléments beaucoup plus lourds (document 1).
Les transformations radioactives qui génèrent des éléments beaucoup plus lourds sont de type β-.
2 – En utilisant le document 2 page suivante, définir le terme « isotope » puis donner la composition du noyau d’uranium le plus représenté à l’état naturel.
Document 2 :
Le numéro atomique de l’élément uranium est Z = 92.
L’uranium naturel se compose de trois isotopes radioactifs : l’uranium 238 de symbole 238U, l’uranium 235 de symbole 235U et l’uranium 234 de symbole 234U.
On remarque que les trois isotopes ont le même numéro atomique Z et un nombre de nucléon différent.
Défini du terme « isotope » : Des isotopes sont des atomes possédant un nombre de proton identique et un nombre de neutron différent (et donc un nombre de nucléon différent).
Composition du noyau d’uranium le plus représenté à l’état naturel ${_{92}^{238}}U$:
- 92 protons
- 238—92=146 neutrons
Document 2 – L’élément uranium
Le numéro atomique de l’élément uranium est Z = 92.
L’uranium naturel se compose de trois isotopes radioactifs : l’uranium 238 de symbole 238U, l’uranium 235 de symbole 235U et l’uranium 234 de symbole 234U. Les proportions de ces trois isotopes sur Terre sont données dans le tableau ci-contre.
| Isotopes | Proportions des isotopes sur Terre |
| Uranium 238U | 99,27 % |
| Uranium 235U | 0,72 % |
| Uranium 234U | 0,01 % |
Source : d’après l’auteur
Document 3 – Évolution du pourcentage de noyaux d’uranium 238 radioactifs dans un échantillon au cours du temps
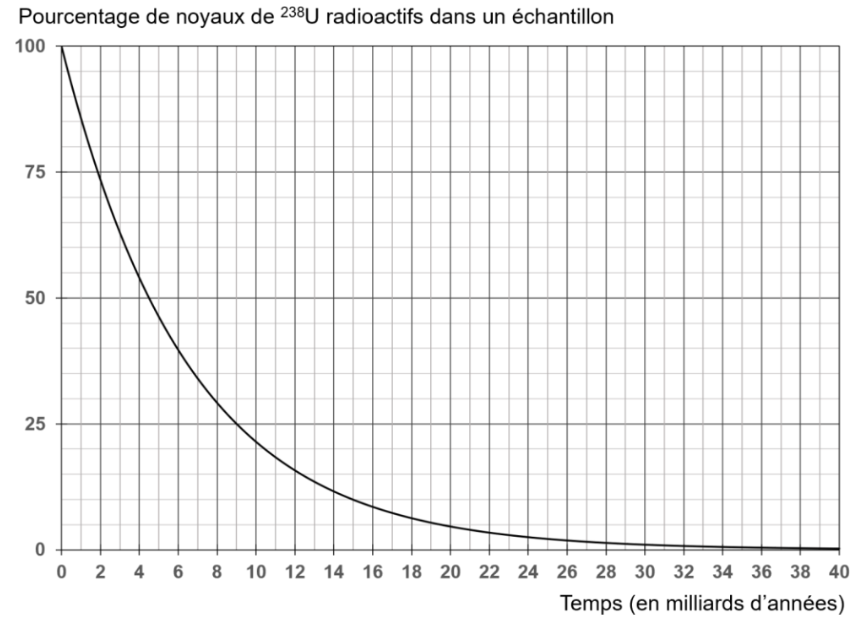
Source : d’après l’auteur
3 – Définir le terme « demi-vie » d’un noyau radioactif.
La demi-vie d’un noyau radioactif est le temps nécessaire pour que la moitié des noyaux radioactifs se désintègrent. Elle est une caractéristique spécifique de chaque isotope radioactif.
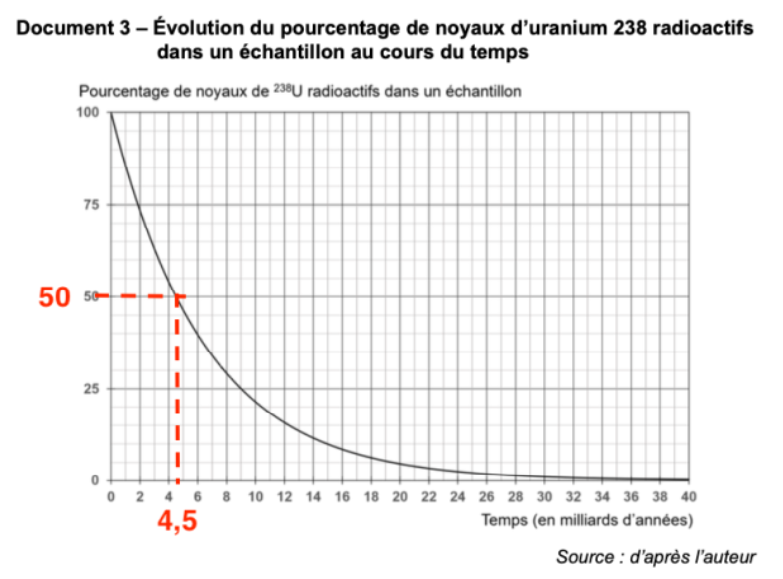
4 – Déterminer graphiquement la valeur de la demi-vie de l’uranium 238 à l’aide du document 3.
Graphiquement, il reste 50% des noyaux radioactifs au bout de 4,5 milliards d’années.
Ainsi : t1/2 = 4,5 milliards d’années.
5 -Proposer une hypothèse expliquant pourquoi nous trouvons encore aujourd’hui de l’uranium 238 sur Terre.
Nous trouvons encore aujourd’hui de l’uranium 238 sur Terre car la Terre à un âge estimé de 4,5 milliards d’années. Ainsi, il reste la moitié de l’uranium 238 initialement présent sur Terre.
Document 4 – L’uraninite, une archive géologique
L’uraninite (photographie ci-contre), de formule UO2 est insoluble dans l’eau.
L’uranium dans cette roche est sous une forme réduite.
Quand l’uranium est sous forme oxydée UO3, il est soluble dans l’eau.
La présence d’uraninite dans un milieu indique donc l’absence de dioxygène dans le milieu en question.

Source de l’image : https://planet-terre.ens- lyon.fr/planetterre/objets/Images/uraninite/uraninite-fig01.jpg
6 -À partir du document 4, préciser une des conditions pour former l’uraninite que l’on retrouve actuellement.
D’après le document 4, L’uraninite est de formule UO2. La présence d’uraninite dans un milieu indique donc l’absence de dioxygène dans le milieu en question.
Ainsi, une des conditions pour former l’uraninite est l’absence de dioxygène dans le milieu.
7 – Sachant que l’on ne trouve plus de gisements d’uranium sédimentaire, formés d’uraninite (UO2), âgés de moins de 2 milliards d’années, préciser l’information apportée par la datation des gisements.
On ne trouve plus de gisements d’uranium sédimentaire, formés d’uraninite (UO2), âgés de moins de 2 milliards d’années.
Cette datation nous informe sur la composition de l’atmosphère qu’il y avait il y a plus de 2 milliards d’années.
Avant 2 milliards d’années, l’atmosphère de la Terre était beaucoup moins riche en oxygène. Cela a permis la formation et la préservation de gisements d’uraninite, puisque l’uranium pouvait rester sous sa forme réduite (UO2) et insoluble.
Après cette période, une augmentation de la concentration d’oxygène dans l’atmosphère s’est produite. Cette augmentation de l’oxygène a conduit à l’oxydation de l’uraninite (UO2) en UO3, qui est soluble dans l’eau, empêchant ainsi la formation de nouveaux gisements d’uraninite après cette période.
Document 5 – Modèle de l’évolution de la pression partielle de certains gaz atmosphériques au cours du temps
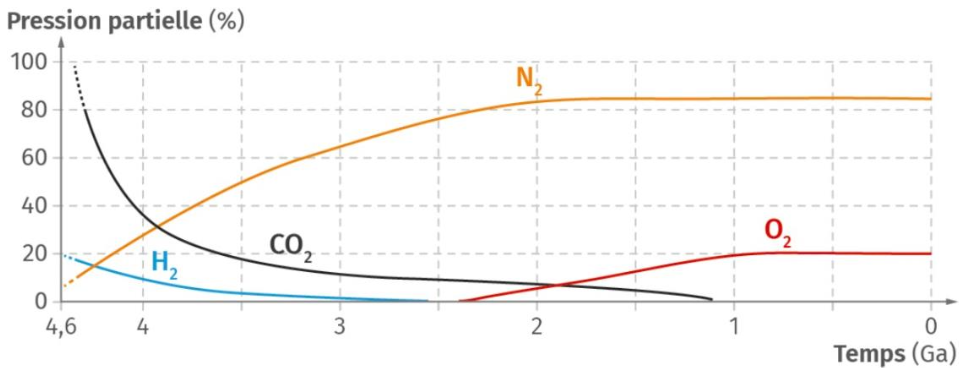
Source : Enseignement scientifique Terminale, lelivrescolaire.fr
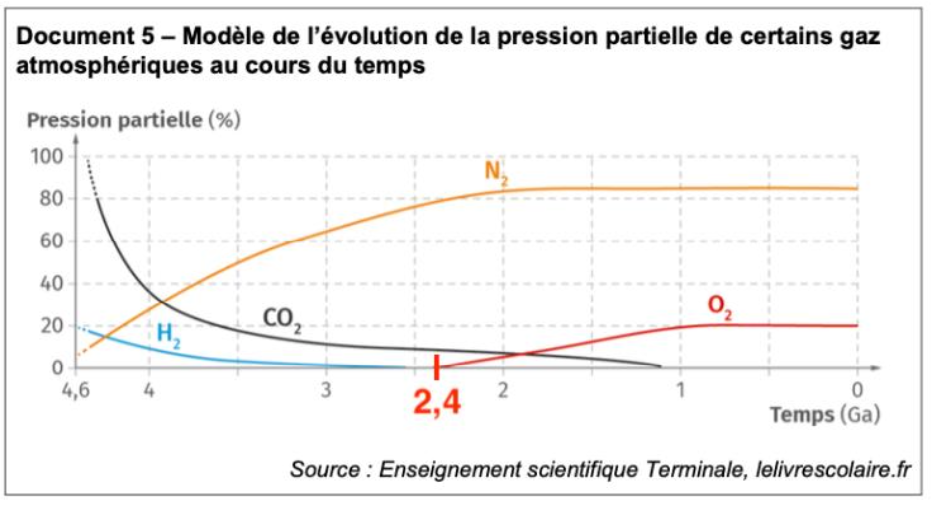
8 – Expliquer en quoi les résultats de l’étude des gisements d’uranium sédimentaires sont compatibles avec l’évolution de la pression partielle en dioxygène dans l’atmosphère du modèle proposé dans le document 5.
Graphiquement, sur le document 5, nous observons que la pression partielle du dioxygène augmente il y a 2,4 milliards d’années.
Avant, il n’y avait pas de dioxygène dans l’atmosphère et la formation d’uraninite (UO2) était possible.
Ainsi, les résultats de l’étude des gisements d’uranium sédimentaires qui indique qu’on ne trouve plus de gisements d’uranium sédimentaire, formés d’uraninite (UO2), âgés de moins de 2 milliards d’années sont compatibles avec l’évolution de la pression partielle en dioxygène dans l’atmosphère du modèle proposé dans le document 5.
9 – Parmi les propositions suivantes, choisir la démarche qui permet de renforcer la validité du modèle proposé dans le document 5 et justifier votre réponse.
Recopier la lettre correspondante.
a – Répliquer des études sur le même échantillon.
b – Obtenir des résultats convergents à partir d’études sur des roches de natures différentes.
c – Rédiger un article scientifique proposé à ses pairs.
La démarche qui permet de renforcer la validité du modèle proposé est :
b- Obtenir des résultats convergents à partir d’études sur des roches de natures différentes.
Cette démarche est importante car elle consiste à tester le modèle sur des échantillons variés pour vérifier si les conclusions obtenues sont consistantes et reproductibles dans différents contextes géologiques.
Si le modèle est valide, il doit être capable d’expliquer les observations dans divers types de roches, pas seulement dans des échantillons spécifiques.
Cette approche renforce la solidité du modèle en démontrant qu’il n’est pas limité à un cas particulier mais s’applique de manière générale.
