Enseignement scientifique Terminale
Durée 1h – 10 points – Thème « Science, climat et société »
Sujet n°ENSSCI3202 et n°ENSSCI3203
Télécharger l’exercice en PDF :
Partie 1 – L’eau sous toutes ses formes
Pour comprendre l’origine des océans, on doit préciser les conditions qui ont permis à l’eau d’exister à l’état liquide sur Terre. En l’état actuel des connaissances, il est admis que l’atmosphère primitive de la Terre présentait des conditions similaires à l’atmosphère actuelle de Vénus.
Document 1 – Diagramme de phase de l’eau
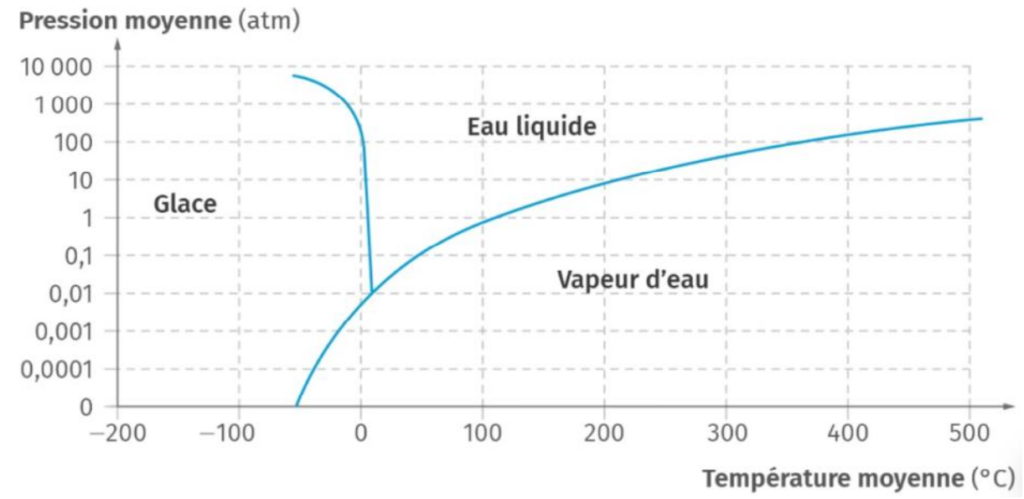
Source : d’après le livre scolaire, enseignement scientifique terminale
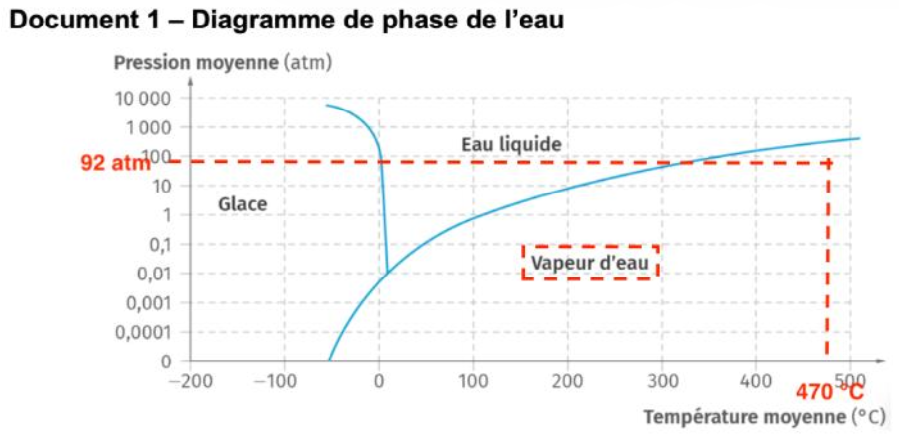
1- Sachant que sur Vénus la pression vaut environ 92 atm et la température 470 °C, expliquer, à l’aide du document 1, pourquoi il n’y a pas d’océans sur Vénus actuellement.
Sur Vénus, où la pression atteint environ 92 atm et la température avoisine les 470 °C, l’eau se trouve sous forme de vapeur. C’est pourquoi il n’y a actuellement pas d’océans sur Vénus.
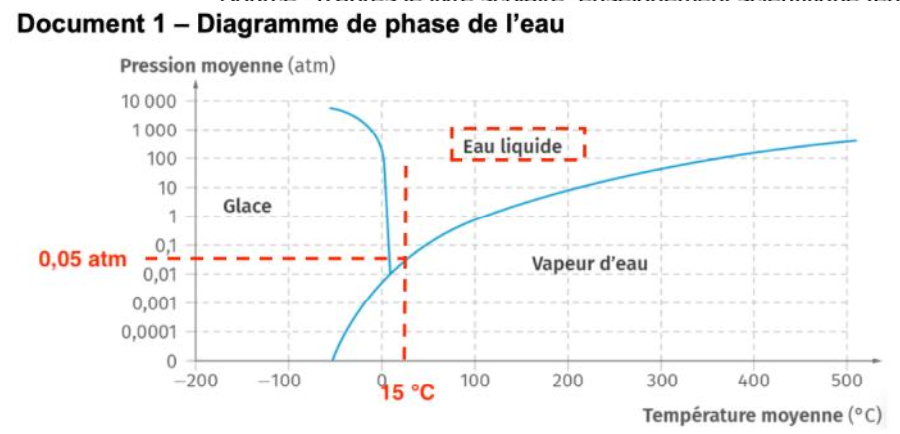
2- Sachant qu’actuellement la température terrestre moyenne est voisine de 15°C, estimer à l’aide du document 1, la plus petite valeur de pression qui permettrait d’obtenir de l’eau liquide sur Terre. Commenter ce résultat.
Graphiquement, Sachant qu’actuellement la température terrestre moyenne est voisine de 15°C, la plus petite valeur de pression qui permettrait d’obtenir de l’eau liquide sur Terre est de 0,05 atm.
Cette pression est très inferieure à la pression atmosphérique terrestre.
L’eau liquide n’a donc pas toujours été présente sur Terre. Sa formation a entraîné une forte évolution de la composition de l’atmosphère terrestre au cours du temps, comme indiqué dans le document 2.
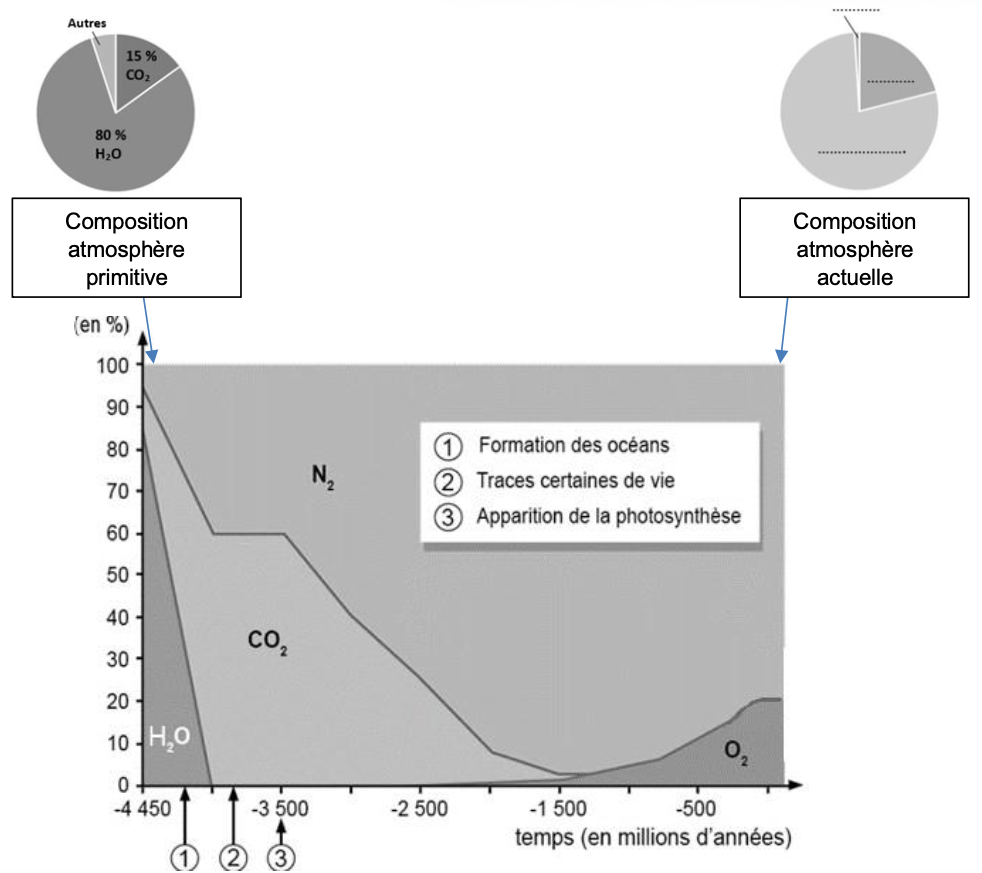
Document 2 – Évolution de la composition de l’atmosphère terrestre au cours des temps géologiques
Source : d’après Ciavatti, 1999
3- Identifier les espèces chimiques de l’atmosphère actuelle et préciser leurs pourcentages.
Espèces chimiques de l’atmosphère actuelle :
Le diazote N2 : 80 % (100-20=80%)
Le dioxygène O2 : 20%
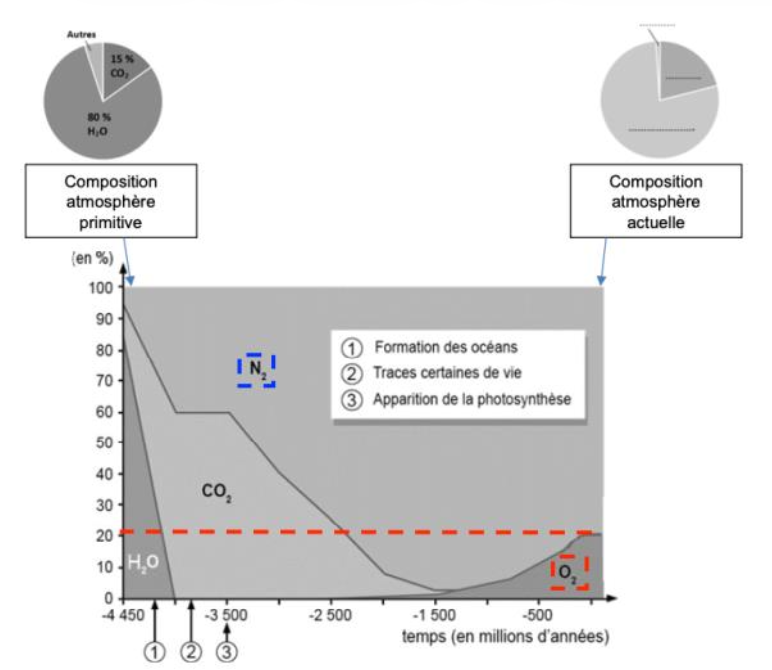
4- Commenter l’évolution du pourcentage de vapeur d’eau dans l’atmosphère primitive et estimer la durée de formation des océans.
Sur le graphique fourni, on constate que la quantité de vapeur d’eau dans l’atmosphère diminue progressivement jusqu’à atteindre 0 % vers -4000 millions d’années.
Cette réduction est liée à la condensation de la vapeur d’eau, qui devient liquide au fur et à mesure que les conditions changent.
Les océans commencent à apparaître un peu avant, vers -4200 millions d’années, lorsque la vapeur d’eau condensée forme les premiers océans.
Partie 2 – Apparition du dioxygène dans l’atmosphère
Document 3 – L’origine du dioxygène dans l’atmosphère terrestre
Les stromatolithes sont des constructions calcaire, réalisées par des bactéries photosynthétiques, que l’on retrouve dans des eaux chaudes et peu profondes, comme actuellement à Shark Bay en Australie.
Ces bactéries utilisent le dioxyde de carbone présent dans l’eau pour produire leur propre matière organique et libérer du dioxygène. Le CO2 consommé modifie l’environnement proche et favorise la précipitation de calcaire CaCO3.
Les roches de la croûte terrestre sont très riches en fer. Le fer sous forme d’ions ferreux Fe2+ est transporté par les eaux, vers les océans. La réaction du fer ferreux avec le dioxygène entraîne un précipité, l’hématite, présent dans les fers rubanés, roches témoignant de l’apparition de la vie il y a 3,2 Ga.
Source : d’après le livre scolaire, enseignement scientifique terminale
5- D’après le document 3, préciser le milieu dans lequel est apparu le dioxygène dans un premier temps.
D’après le document 3, le dioxygène est apparu dans un premier temps dans les eaux chaudes et peu profondes, où les stromatolithes, formés par des bactéries photosynthétiques, se développaient.
Ces bactéries utilisaient le dioxyde de carbone (CO2) présent dans l’eau pour produire de la matière organique et libérer du dioxygène au cours de la photosynthèse.
6- Parmi les équations des réactions chimiques suivantes, recopier sur votre copie celle qui correspond à la réaction permettant la production du dioxygène, puis nommer cette réaction métabolique :
- 4 Fe + 3 O2 → 2 Fe2O3
- 2 Fe(OH)3 → Fe2O3 + 3 H2O
- n CO2 + n H2O → CnH2nOn + n O2
- CnH2nOn + n O2 → n CO2 + n H2O
L’équation qui correspond à la réaction permettant la production du dioxygène est :
c) nCO2 +nH2O→CnH2nOn +nO2
Cette réaction métabolique s’appelle la photosynthèse.
Partie 3 – Transformation du dioxygène atmosphérique
Document 4 – Schéma des étapes permettant la formation de l’ozone
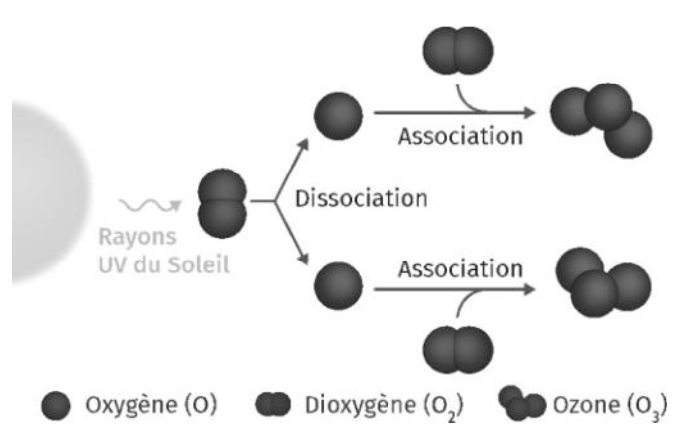
Source : d’après Le livre scolaire, enseignement scientifique terminale
7- Traduire le schéma du document 4, sous forme d’équations de réactions chimiques. Les deux étapes de la formation de l’ozone stratosphérique sont attendues (dissociation et association).
Sur le schéma du document 4, lors de la dissociation, une molécule de dioxygène se sépare en deux atomes d’oxygène :
O2 → 2O
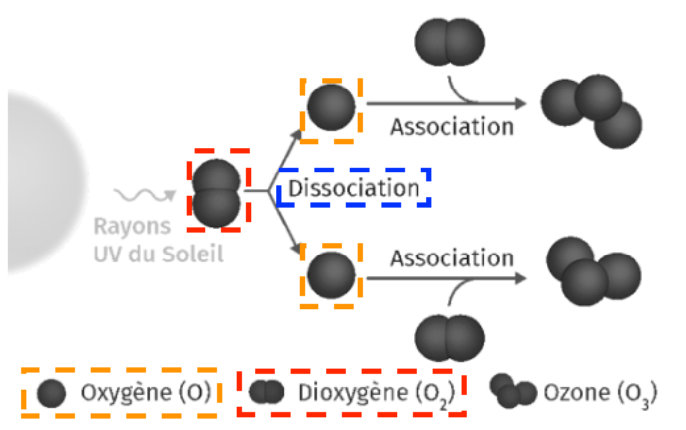
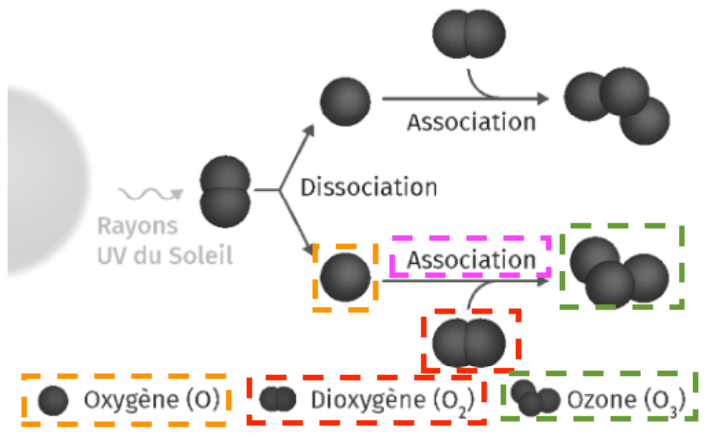
Sur le schéma du document 4, lors de l’association, une molécule de dioxygène réagit avec un atome d’oxygène pour donner de l’ozone :
O2 + O → O3
Document 5 – Graphique de la quantité de lésion de l’ADN en fonction des UV
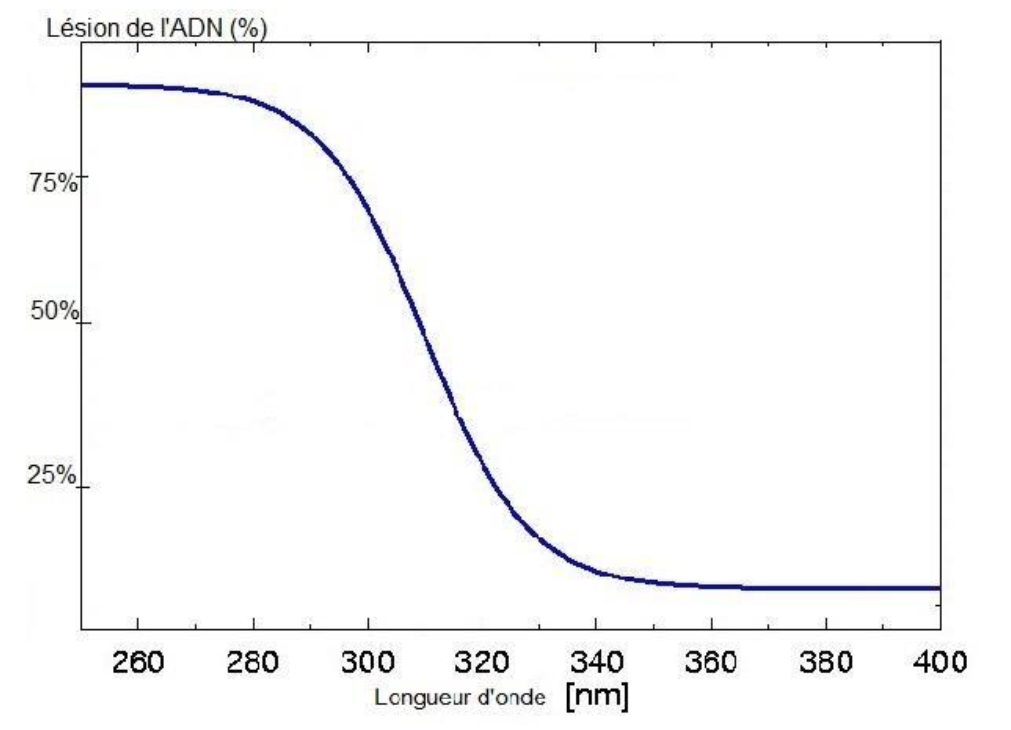
Source : d’après ENS Lyon 2021, d’après la caractérisation de l’ADN par Marie Orrego 2013
Document 6 – Graphique mettant en évidence l’importance de l’ozone dans l’absorption des rayonnements ultraviolets
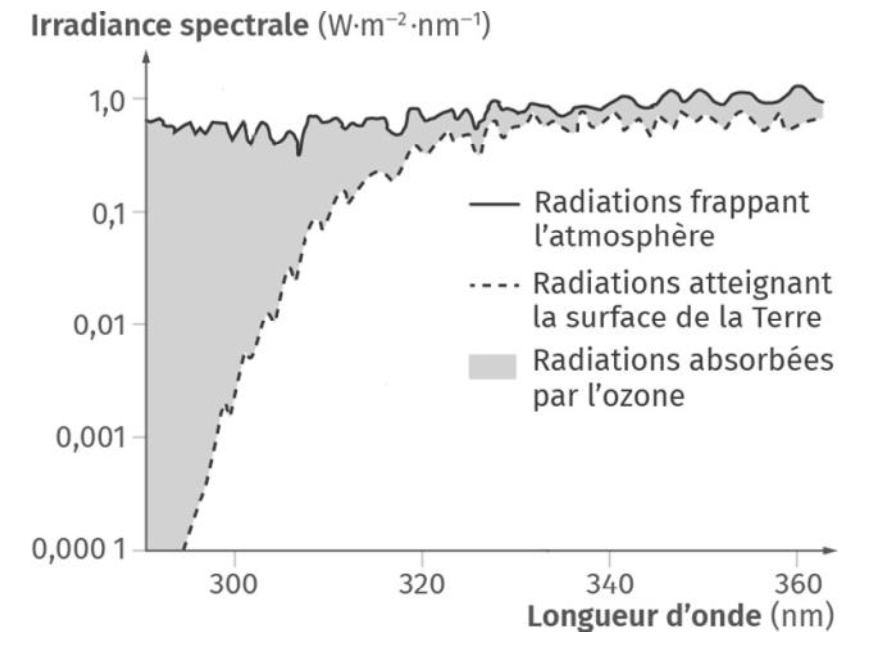
Source : D’après le livre scolaire, enseignement scientifique terminale
Le 16 septembre, le monde célébrera la Journée internationale de la protection de la couche d’ozone. Le Protocole de Montréal, adopté en 1987 et entré en vigueur en 1989, est considéré comme l’une des plus grandes réussites au monde en matière de traités environnementaux. L’accord a permis une réduction importante des émissions de substances appauvrissant la couche d’ozone. Les données indiquent que la couche d’ozone se régénère et devrait se rétablir d’ici au milieu du XXIe siècle.
8- À partir des documents 5 et 6 et de vos connaissances, argumenter en faveur des mesures mondiales prises pour préserver la couche d’ozone.
Le graphique du document 5 montre que les dommages à l’ADN sont très élevés quand la longueur d’onde inférieure à 300 nm.
Le document 6 montre que la couche d’ozone filtre ces rayons nocifs.
Le Protocole de Montréal, adopté en 1987, a permis de réduire les émissions de substances destructrices pour l’ozone, contribuant ainsi à la régénération de cette couche vitale pour les êtres vivants.
Cet accord est un succès qui montre l’efficacité des actions internationales pour préserver notre environnement.
