Enseignement scientifique Terminale
Durée 1h – 10 points – Thème « Science, climat et société »
Sujet n°ENSSCI3178 et n°ENSSCI3183
Télécharger l’exercice en PDF :
Partie 1 – L’évolution de la quantité de dioxygène dans l’atmosphère
Contrairement à l’atmosphère actuelle, l’atmosphère primitive était totalement dépourvue de dioxygène. Bien que présent dans les océans dès – 3,5 milliards d’années, ce gaz n’apparaît dans l’atmosphère que vers – 2,4 milliards d’années.
1- D’après l’expérience présentée dans le document 1 suivant, indiquer à quelle condition un précipité rouge d’hydroxyde de fer peut se former. Justifier.
Résultats d’une expérience d’oxydation des ions Fe2+ :
- Sans dioxygène, la solution verte contenant des ions Fe2+ ne subit aucune réaction chimique.
- Avec dioxygène, la solution verte contenant des ions Fe2+ devient incolore (les ions Fe2+ réagissent) et un précipité rouge d’hydroxyde de fer apparait.
Ainsi, un précipité rouge d’hydroxyde de fer peut se former uniquement en présence de dioxygène.
Document 1 – Ions Fe2+ et dioxygène
Exploités comme gisements de fer, les formations de fer rubanés sont des roches sédimentaires formées en grandes quantités dans les océans entre – 3,8 et – 2,2 milliards d’années. Elles contiennent du fer à l’état oxydé, issu de l’oxydation du fer qui était présent à l’époque dans les océans sous forme d’ions Fe2+.
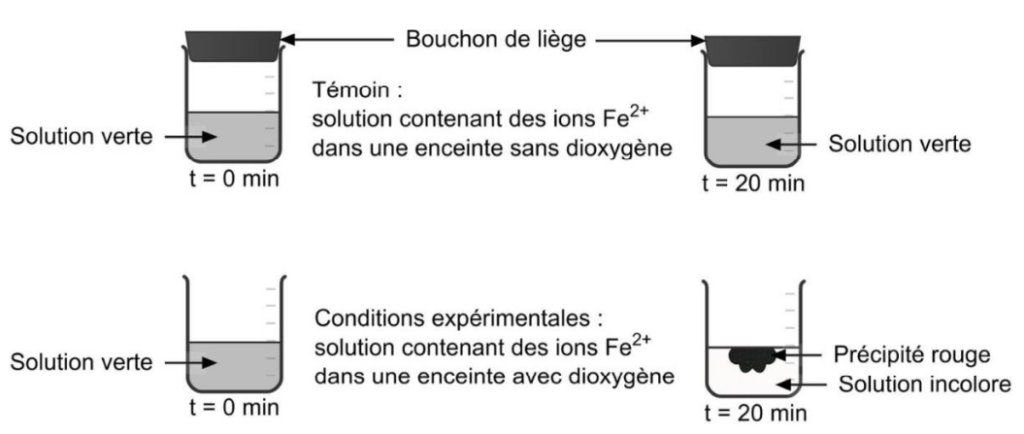
Figure B – Résultats d’une expérience d’oxydation des ions Fe2+
Source : schémas réalisés par l’auteur
Lors de l’altération par l’eau des roches continentales, des ions Fe2+ sont libérés. Ils sont transportés sous forme soluble jusque dans les océans. En présence d’oxygène, ils s’oxydent en ions Fe3+ qui précipitent sous forme d’hydroxyde de fer (précipité rouge). Ce précipité s’accumule au fond des océans et forme les fers rubanés.
Remarque : à l’époque de la formation des fers rubanés, l’atmosphère primitive était réductrice (dépourvue de dioxygène).
2- Analyser le document 2 page suivante et relier la chronologie de formation des fers rubanés à l’évolution de la teneur atmosphérique en dioxygène.
Le document 2 montre que jusqu’à environ -2,4 milliards d’années, la teneur en dioxygène atmosphérique est quasiment nulle.
A partir de -2,4 milliards d’années on observe une augmentation brutale du taux de dioxygène dans l’atmosphère.
D’après le document 1, les fers rubanés se sont formés entre -3,8 et -2,2 milliards d’années, avant cette hausse du dioxygène.
Le dioxygène produit réagissait avec les ions Fe²⁺ dissous pour former des précipités d’hydroxyde de fer (fers rubanés).
Lorsque tout le fer dissous a été oxydé que le dioxygène s’est accumulé dans l’atmosphère.
3- À l’aide des documents 1 et 2, proposer une explication à la fin de la formation des fers rubanés après 2,2 milliards d’années.
D’après les documents 1 la formation des fers rubanés nécessite la présence d’ions Fe²⁺ dans l’eau et de dioxygène pour provoquer leur oxydation en Fe³⁺, formant ainsi un précipité rouge d’hydroxyde de fer.
Le document 2 montre qu’à partir de -2,4 milliards d’années, la concentration de dioxygène dans l’atmosphère augmente fortement.
La fin de la formation des fers rubanés vers -2,2 milliards d’années s’explique par l’épuisement du fer dissous dans les océans, empêchant la poursuite du processus de précipitation malgré la présence de dioxygène.
Document 2 – Évolution du dioxygène atmosphérique
L’analyse chimique des roches très anciennes a permis d’établir les taux de dioxygène atmosphérique au cours de l’histoire de la Terre.
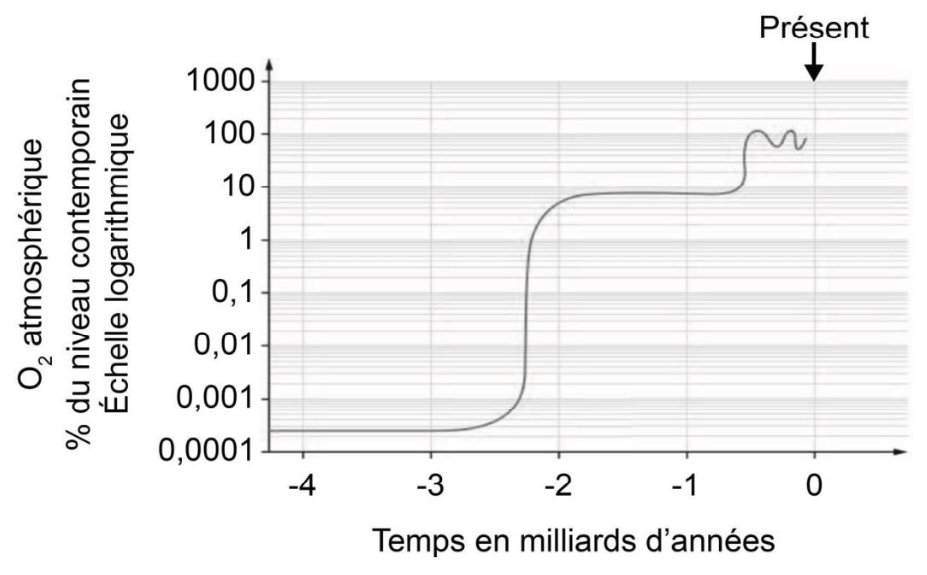
Figure C – Évolution du taux de dioxygène atmosphérique au cours des temps géologiques
Source : Campbell, 2012
Document 3 – Formation de la rouille
La rouille se forme à partir du fer (ou d’alliage contenant du fer comme l’acier). On cherche à comprendre le rôle du dioxygène de l’atmosphère dans la formation de la rouille à partir de fer. On place pour cela de la laine de fer dans une éprouvette humidifiée retournée sur de l’eau. Cette dernière a été préalablement bouillie pour retirer tous les gaz dissous qu’elle pouvait contenir. On réalise alors trois expériences schématisées ci-dessous.
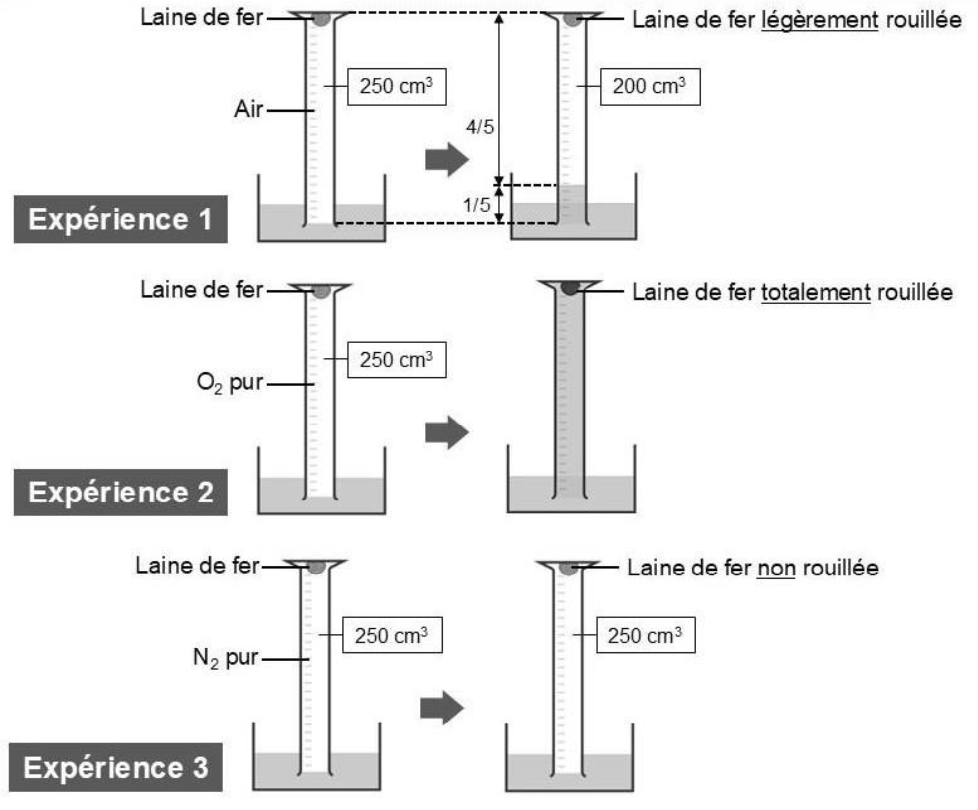
Figure D – Les expériences et leurs résultats
Source : schémas réalisés par l’auteur
4- Montrer, à l’aide du document 3, que l’atmosphère actuelle est composée d’environ un cinquième de dioxygène en volume.
Dans l’expérience 2, réalisée avec 250 cm³ de dioxygène pur, on observe que tout le dioxygène est consommé et que la laine de fer est totalement rouillée.
Cela montre que le dioxygène réagit avec le fer pour former de la rouille.
Dans l’expérience 3, réalisée avec 250 cm³ de diazote pur, aucune rouille ne se forme : la laine de fer reste intacte.
Cela montre que le diazote ne réagit pas avec le fer.
Dans l’expérience 1, avec 250 cm³ d’air, la laine est légèrement rouillée et il reste 200 cm³ de gaz.
Sachant que l’air est composé de dioxygène et de diazote et que seul le dioxygène réagit avec le fer pour former de la rouille.
On en déduit que la différence de 50 cm³ correspond donc volume de dioxygène consommé.
Proportion de dioxygène dans l’air = $\frac{50}{250}=\frac{1}{5}$
Ainsi, l’atmosphère actuelle est composée d’environ un cinquième de dioxygène en volume.
Partie 2 – La contribution des cyanobactéries à l’évolution de la composition de l’atmosphère
Document 4 – Cyanobactéries et formation des stromatolithes
Les stromatolites sont des bioconstructions calcaires que l’on retrouve dans des milieux marins chauds et peu profonds. Ils sont créés par des cyanobactéries. Les plus anciens ont été datés de 3,5 milliards d’années.
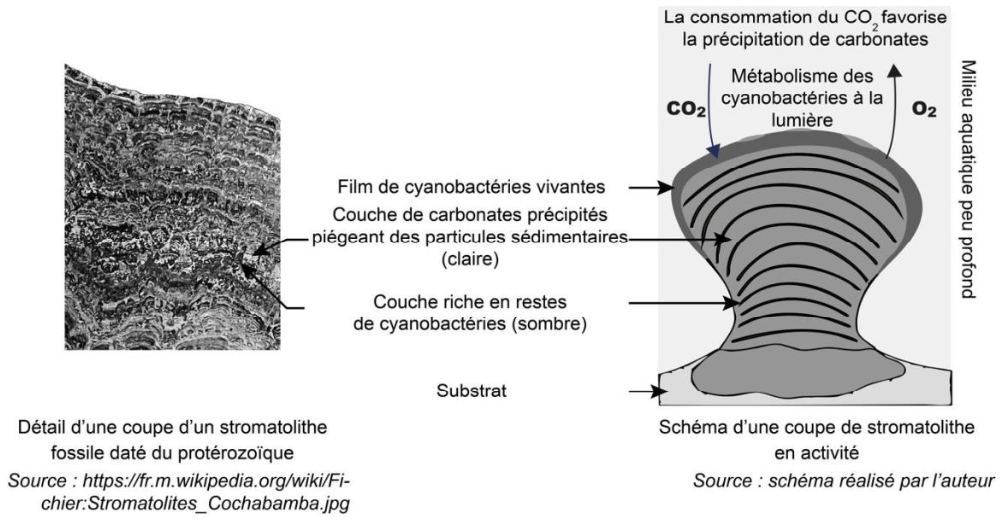
Figure F – Organisation et fonctionnement d’un stromatolithe
Dans une eau chaude et peu profonde, les cyanobactéries contenues dans les stromatolithes fabriquent leurs propres molécules organiques selon la réaction chimique suivante :
CO2 + H2O → glucides + O2
Cette réaction chimique, en consommant du CO2, favorise la précipitation des ions carbonates (HCO−) sous forme de calcaire (CaCO3) :
2 HCO− + Ca2+ → CaCO3 + CO2 + H2O
Figure C – Cyanobactéries actuelles observées au microscope
5- À partir du document 4 et de vos connaissances, donner le nom de la réaction chimique pratiquée par les cyanobactéries permettant la synthèse de molécules organiques.
La réaction CO₂ + H₂O → glucides + O₂ correspond à la photosynthèse.
Ainsi, la réaction chimique pratiquée par les cyanobactéries permettant la synthèse de molécules organiques est la photosynthèse.
6- L’atmosphère primitive de la Terre était totalement dépourvue de dioxygène. Indiquer l’origine probable de l’augmentation de la quantité de dioxygène dans l’atmosphère. Justifier.
D’après le document 4, les cyanobactéries sont présentes dès -3,5 milliards d’années.
Avec la photosynthèse, elles produisent du dioxygène.
Dans un premier temps, le dioxygène libéré a été consommé pour oxyder les ions Fe²⁺ des océans (formation des fers rubanés).
Après l’épuisement du fer dissous que le dioxygène a pu s’accumuler durablement dans l’atmosphère, entraînant son enrichissement progressif en O₂.
7- À l’aide de la réponse à la question 6 et de la figure C du document 2, justifier que l’apparition des êtres vivants a contribué à l’évolution de la composition de l’atmosphère terrestre en favorisant une hausse de la teneur en dioxygène et une baisse de la teneur en dioxyde de carbone.
Les cyanobactéries, premiers êtres vivants apparus sur Terre, réalisent la photosynthèse, un processus qui consomme du dioxyde de carbone (CO₂) et produit du dioxygène (O₂).
La figure C du document 2 montre une augmentation de la teneur en dioxygène à partir de -2,4 milliards d’années.
L’apparition des êtres vivants photosynthétiques donne naissance au dioxygène. Celui-ci précipite d’abord les ions fer, et une fois que tout le fer a été précipité, le dioxygène s’accumule dans l’atmosphère.
La réaction chimique de la photosynthèse, CO₂ + H₂O → glucides + O₂, implique une consommation de CO₂, ce qui a contribué à diminuer progressivement sa teneur dans l’atmosphère.
Ainsi, l’apparition des êtres vivants a contribué à l’évolution de la composition de l’atmosphère terrestre en favorisant une hausse de la teneur en dioxygène et une baisse de la teneur en dioxyde de carbone.
8- En vous appuyant sur cet exemple et au moins un autre exemple issu de vos connaissances, expliquer comment les scientifiques parviennent à reconstituer les environnements du passé alors qu’ils ne disposent d’aucune mesure directe. Indiquer les types d’indices utilisés et préciser comment les scientifiques les interprètent.
Les preuves indirectes sont des témoins qui conservent des informations sur les conditions environnementales anciennes, et les chercheurs utilisent des méthodes rigoureuses pour les analyser et en tirer des conclusions.
Par exemple, l’étude des roches sédimentaires, qui se forment dans des conditions spécifiques (par exemple, en présence d’oxygène), permet de reconstruire des événements géologiques, comme l’oxygénation de l’atmosphère par les cyanobactéries.
Les carottes glaciaires sont un autre exemple d’indice pour reconstituer le passé, même sans mesures directes. En forant des couches de glace, les scientifiques peuvent analyser les bulles d’air piégées dans la glace, qui contiennent des échantillons d’atmosphère datant de millions d’années.
Ces analyses, combinées à des modèles scientifiques, permettent de faire des hypothèses solides même en l’absence de données directes.
La rigueur de ces méthodes repose sur la cohérence entre différentes sources d’indices et leur capacité à reproduire des événements connus à partir d’observations actuelles.
Ainsi, les scientifiques parviennent à reconstituer les environnements du passé en se basant sur des preuves indirectes.


