Bac Polynésie 2023 Sujet 1
Exercice 1 – (9 points) – Durée 1h35 – Calculatrice autorisée
Sujet n°23-PYCJ1PO1
Sujet et corrigé
EXERCICE 1 – UN CHIMISTE QUI MÉRITE D’ÊTRE CONNU : KARL FRIEDRICH MOHR (9 points).
Karl Friedrich Mohr est un chimiste allemand ayant vécu au dix-neuvième siècle. Il a introduit de nombreuses techniques qui ont fait progresser la chimie expérimentale. Ses découvertes restent utiles chaque jour dans les laboratoires du monde entier.
L’objectif de cet exercice est d’illustrer, à travers trois exemples, les principaux apports de Mohr à la chimie : le sel de Mohr, le chauffage à reflux et le dosage par titrage.
Le sel de Mohr.
Les ions fer (II) Fe2+(aq) sont facilement oxydés en ions fer (III) Fe3+(aq) par le dioxygène de l’air qui se dissout en solution aqueuse. Pour minimiser cette oxydation et permettre la conservation d’une solution d’ions fer (II), Mohr a proposé d’utiliser un solide ionique hydraté de formule chimique : (NH4)2Fe(SO4)2, 6H2O(s). En son honneur, ce solide est nommé le « sel de Mohr ».
Données :
- Masses molaires atomiques :
M(H) = 1,0 g·mol–1, M(N) = 14,0 g·mol–1, M(O) = 16,0 g·mol–1,
M(S) = 32,1 g·mol–1, M(Fe) = 55,8 g·mol–1 ;
- Le sel de Mohr contient des ions ammonium NH4+, des ions fer (II) Fe2+ et des ions sulfate SO42-.
Q1. Écrire les demi-équations électroniques des couples oxydant-réducteur Fe3+(aq)/Fe2+(aq) et O2(aq)/H2O(l). Utiliser ces demi-équations pour justifier l’équation de la réaction qui modélise l’oxydation des ions fer (II) par le dioxygène en milieu acide :
4Fe2+(aq) + O2(aq) + 4H+(aq) → 4Fe3+(aq) + 2H2O(l)
Couple ${\rm Fe}^{3+}(aq)/{\rm Fe}^{2+}(aq)$ :
$${\rm Fe}^{3+}(aq)+e^-={\rm Fe}^{2+}(aq)$$
Couple $O_2(aq)/H_2O(l)$ :
$$O_2(aq)+4H^++4e^-=2H_2O(l)$$
Oxydation du fer ${\rm Fe}^{2+}(aq)$ par le dioxygène $O_2(aq)$ :
$${\rm Fe}^{2+}\left(aq\right)={\rm Fe}^{3+}\left(aq\right)+e^-\ \ \ \ \ \ \ \ \ \ \ \ \ \times 4$$
$$O_2(aq)+4H^++4e^-=2H_2O(l)$$
$$4{\rm Fe}^{2+}\left(aq\right)+O_2(aq)+4H^+\rightarrow4{\rm Fe}^{3+}\left(aq\right)+2H_2O(l)$$
On prépare un volume V de valeur égale à 100,0 mL d’une solution aqueuse de sel de Mohr en dissolvant une masse m de solide de valeur égale à 2,00 g. L’équation suivante permet de modéliser la dissolution du sel de Mohr dans l’eau :
(NH4)2Fe(SO4)2, 6H2O(s) → 2NH4+(aq) + Fe2+(aq) + 2SO42-(aq) + 6H2O(l)
Q2. Vérifier que la valeur de la masse molaire Msel du sel de Mohr est égale à 392,0 g·mol–1.
$M_{sel}=M(\left(NH_4\right)2Fe\left(SO_4\right)2,6H_2O)$
$M{sel}=2M\left(N\right)+2\times 4M\left(H\right)+M\left(Fe\right)+2M\left(S\right)+2\times 4M\left(O\right)+6\times 2M\left(H\right)+6M\left(O\right)$
$M{sel}=2\times 14,0+2\times 4\times 1,0+55,8+2\times 32,1+2\times 4\times 16,0+6\times 2\times 1,0+6\times 16,0$
$M_{sel}=392,0\ g.{\rm mol}^{-1}$
Q3. Calculer la valeur de la concentration c en soluté apporté. Montrer alors l’intérêt du sel de Mohr en expliquant comment on peut connaitre simplement la concentration en quantité de matière [Fe2+] des ions fer (II) présents dans la solution obtenue.
$c=\frac{n}{V}$
Or
$n=\frac{m}{M}$
D’ou
$c=\frac{\frac{m}{M}}{V}$
$c=\frac{m}{M\times V}$
$c=\frac{2,00}{392,0\times 100,0{\times 10}^{-3}}$
$c=5,10{\times 10}^{-2}\ mol.L^{-1}$
$$\left(NH_4\right)_2Fe\left(SO_4\right)_2,6H_2O\left(s\right)\rightarrow2{\rm NH}_4^+\left(aq\right)+{\rm Fe}^{2+}\left(aq\right)+2{\rm SO}_4^{2-}\left(aq\right)+6H_2O\left(l\right)$$
Le coefficient stœchiométrique devant ${\rm Fe}^{2+}$ vaut 1, ainsi :
$\left[{\rm Fe}^{2+}\right]=c$
Ainsi, on peut connaître simplement la concentration des ions fer (II) qui est identique à c du sel de Mohr d’où son intérêt.
Le chauffage à reflux.
Mohr a mis au point le dispositif dit du « chauffage à reflux », représenté figure 1, qui a révolutionné la chimie de synthèse.
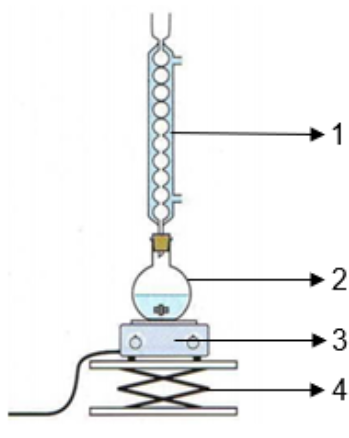
Figure 1. Montage du chauffage à reflux.
Q4. Nommer sur la copie les éléments du montage de la figure 1 numérotés de 1 à 4.
| 1 | Réfrigérant à boule |
| 2 | ballon |
| 3 | chauffe ballon |
| 4 | support élévateur |
On s’intéresse à la synthèse d’un ester à l’odeur de rhum : le méthanoate d’éthyle. Le mélange réactionnel est constitué d’un volume VAc d’une valeur égale à 7,0 mL d’acide méthanoïque, d’un volume VAl d’une valeur égale à 10,0 mL d’éthanol et de quelques gouttes d’acide sulfurique concentré. La transformation d’estérification qui se déroule dans le ballon peut être modélisée par l’équation de réaction suivante :
HCO2H(l) + C2H6O(l) ⇄ HCO2C2H5(l) + H2O(l)
Tableau de données :
| Espèce chimique | Formule semi-développée et masse molaire moléculaire | Température d’ébullition | Pictogramme(s) de sécurité |
| Acide méthanoïque | 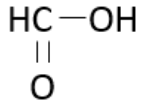 MAc = 46,0 g·mol–1 MAc = 46,0 g·mol–1 | 100,7°C |  |
| Éthanol | 78,5°C |  | |
| Méthanoate d’éthyle | 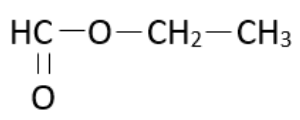 MEs = 74,0 g·mol–1 MEs = 74,0 g·mol–1 | 54,3°C |  |
Q5. Nommer les groupes caractéristiques présents dans ces trois molécules.
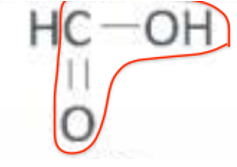
Acide méthanoïque :
Groupe carboxyle
éthanol :
Groupe hydroxyle
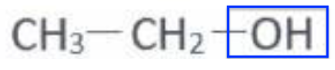
Méthanoate d’éthyle :
Groupe carboxyle ou ester
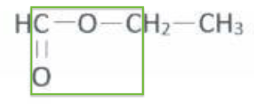
Q6. Représenter la formule topologique du méthanoate d’éthyle.
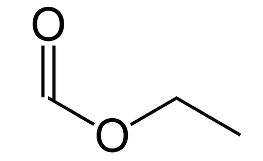
Q7. Citer deux avantages d’un chauffage à reflux et indiquer une précaution à respecter pour réaliser cette synthèse.
Le chauffage à reflux permet :
- d’accélérer la réaction
- sans perte de matière
Une précaution à respecter pour réaliser cette synthèse est de porter des gants car l’acide sulfurique est corrosif.
Q8. Indiquer le rôle joué par l’acide sulfurique qui n’apparaît pas dans l’équation de la réaction de synthèse.
L’acide sulfurique qui n’apparaît pas dans l’équation de la réaction de synthèse : c’est un catalyseur. Il permet d’accélérer la réaction.
Données :
- Masse volumique de l’acide méthanoïque : ρAc = 1,22 g·mL–1 ;
- Masse volumique de l’éthanol : ρAl = 0,79 g·mL–1 ;
Q9. À l’aide des données, calculer les valeurs des quantités de matière en acide méthanoïque nAc et en alcool nAl des réactifs dans l’état initial. Justifier que l’éthanol est le réactif limitant.
$n=\frac{m}{M}$
Or
$\rho=\frac{m}{V}$
$m=\rho\times V$
$n=\frac{\rho\times V}{M}$
$n_{Ac}=\frac{\rho_{Ac}\times V_{Ac}}{M_{Ac}}$
$n_{Ac}=\frac{1,22\times 7,0}{46,0}$
$n_{Ac}=1,86{\times 10}^{-1}\ mol$
$n_{Al}=\frac{\rho_{Al}\times V_{Al}}{M_{Al}}$
$n_{Al}=\frac{0,79\times 10,0}{46,0}$
$n_{Al}=1,72{\times 10}^{-1}\ mol$
$x_{max1}=\frac{n_{Ac}}{1}=1,86{\times 10}^{-1}\ mol$
$x_{max2}=\frac{n_{Al}}{1}=1,72{\times 10}^{-1}\ mol$
$x_{max}=x_{max2}=1,72{\times 10}^{-1}\ mol $ : l’éthanol est le réactif limitant.
Q10. Dans les conditions de l’expérience, la valeur du rendement R de la synthèse est égale à 0,70. Calculer la valeur de la masse d’ester m produite dans ces conditions.
$R=\frac{m_{Es}^{produite}}{m_{Es}^{maximale}}$
$\frac{m_{Es}^{produite}}{m_{Es}^{maximale}}=R$
$m_{Es}^{produite}=R\times m_{Es}^{maximale}$
Or
$m_{Es}^{maximale}=n_{Es}^{maximale}\times M_{Es}$
D’ou
$m_{Es}^{produite}=R\times n_{Es}^{maximale}\times M_{Es}$
Or
$n_{Es}^{maximale}=x_{max}$
D’ou
$m_{Es}^{produite}=R\times x_{max}\times M_{Es}$
$m_{Es}^{produite}=0,7\times 1,72{\times 10}^{-1}\times 74,0$
$m_{Es}^{produite}=8,90\ g$
Pour optimiser le rendement de cette synthèse, il est possible de mettre en œuvre un montage de distillation fractionnée représenté figure 2.
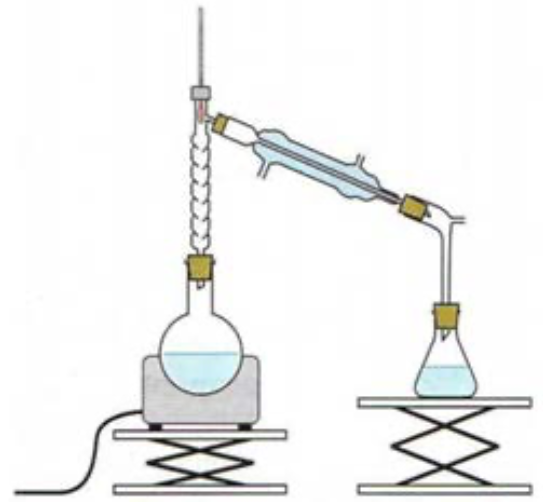
Figure 2. Montage de distillation fractionnée.
Q11. À l’aide des températures d’ébullition fournies dans le tableau de données, expliquer en quoi le montage de distillation fractionnée permet d’optimiser le rendement de la synthèse du méthanoate d’éthyle.
Le méthanoate d’éthyle est celui qui à la température d’ébullition la plus basse (celle de l’eau est 100°C).
Le montage de distillation fractionnée permet au méthanoate d’éthyle de s’évaporer une fois produite.
Il ne peut plus alors réagir avec l’eau. La réaction inverse ne peut plus se produire : le rendement augmente.
Le montage de distillation fractionnée permet donc d’optimiser le rendement de la synthèse du méthanoate d’éthyle.
Le dosage par titrage.
Karl Friedrich Mohr est l’inventeur de la technique du dosage par titrage qui met en jeu une transformation chimique afin de déterminer la quantité de matière d’une espèce chimique en solution. Il a conçu l’outil essentiel de cette technique : la burette graduée fermée en son extrémité inférieure par un robinet ou par une « pince de Mohr » (figure 3).

Figure 3. Burette de Mohr dans un dispositif historique de dosage par titrage.
On dispose de deux solutions pour réaliser un dosage par titrage :
- Solution S1 de chlorure de potassium (K+(aq) ; Cl–(aq)) de concentration en quantité de matière en ions chlorure c1 et de volume V1 = 200,0 mL.
- Solution S2 de nitrate d’argent (Ag+(aq) ; NO3–(aq)) de concentration en quantité de matière c2 = 0,080 mol·L–1.
On souhaite connaitre la concentration c1 en quantité de matière en ions chlorure.
Q12. Parmi les solutions S1 et S2, identifier la solution titrée et la solution titrante. Puis indiquer quelle solution doit être placée dans la burette.
Solution titrée : on cherche à déterminer sa concentration : Solution S1 de chlorure de potassium (K+(aq) ; Cl–(aq))
Solution titrante : on connaît sa concentration : Solution S2 de nitrate d’argent (Ag+(aq) ; NO3–(aq))
On place dans la burette la solution titrante : Solution S2.
La solution S2 de nitrate d’argent est versée lentement. La réaction support du titrage est une réaction qui produit un précipité blanc de chlorure d’argent :
Ag+(aq) + Cl–(aq) → AgCl(s)
Dans le cas d’un dosage par titrage des ions chlorure, Mohr a montré que l’équivalence pouvait être repérée en présence de chromate de potassium par l’apparition d’un précipité rouge brique. On nomme cette technique de dosage par titrage particulière la « méthode de Mohr ».
Le précipité rouge apparaît pour un volume V2E de solution S2 versé de valeur égale à 7,5 mL.
Q13. Définir l’équivalence d’un dosage par titrage puis, en exposant votre raisonnement, calculer la valeur de la concentration en quantité de matière en ions chlorure c1.
L’équivalence est atteinte lorsque les réactifs sont introduits dans des proportions stœchiométriques.
A l’équivalence :
$$\frac{n_{{\rm Cl}^-}^i}{1}=\frac{n_{{\rm Ag}^+}^{eq}}{1}$$
$$c_1\times V_1=c_2\times V_{2E}$$
$$c_1=\frac{c_2\times V_{2E}}{V_1}$$
$$c_1=\frac{0,080\times 7,5\times {10}^{-3}}{200,0\times {10}^{-3}}$$
$$c_1=3,0\times {10}^{-3}mol{.L}^{-1}$$
Il est possible aussi de déterminer la concentration en quantité de matière des ions chlorure c1 par un dosage par titrage conductimétrique. Si l’on mesure la conductivité du mélange réactionnel durant la transformation chimique, on obtient la courbe de la figure 4.
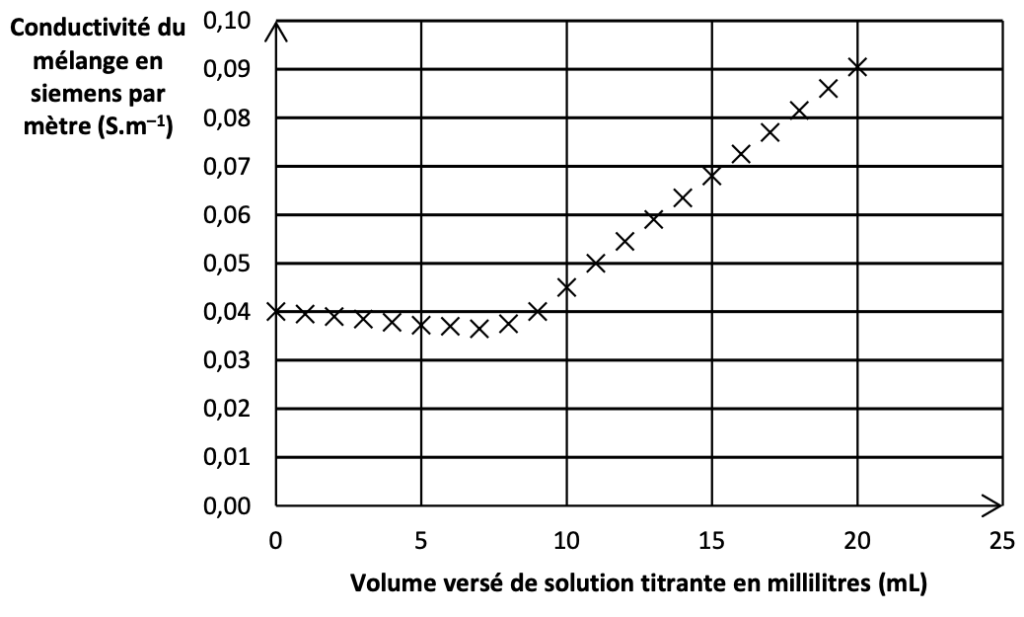
Figure 4. Courbe de dosage par titrage conductimétrique.
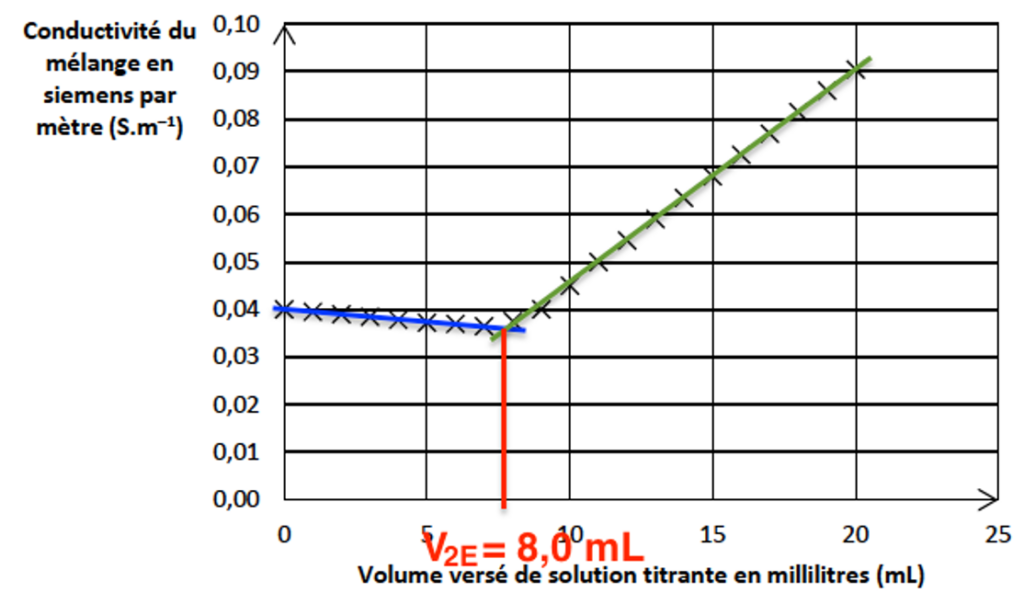
Q14. Expliquer comment cette courbe permet d’obtenir le volume V2E de solution titrante versée à l’équivalence du dosage par titrage.
On repère l’équivalence au croisement des deux portions de droite.
Graphiquement : $V_{2E}=8,0\ mL.$
Données :
- Conductivité σ d’une solution ionique (loi de Kohlrausch) : σ = ∑i λi × [ion]i ;
- Conductivités molaires ioniques λi en mS·m2·mol–1 à 25°C :
| K+ | Cl– | Ag+ | NO3– |
| 7,3 | 7,6 | 6,2 | 7,1 |
Q15. À l’aide des données, justifier sans calcul l’allure de la courbe de la figure 4.
$${\rm Ag}{(aq)}^++{\rm Cl}{(aq)}^-\rightarrow{\rm AgCl}_{(s)}$$
Avant l’équivalence :
les ions ${\rm Ag}^+$ sont ajoutés et consommés immédiatement, ils constituent le réactif limitant, la concentration des ions ${\rm Ag}^+$ est nulle.
les ions ${\rm NO}_3^-$ sont ajoutés, ils ne réagissent pas, la concentration des ions ${\rm NO}_3^-$ augmente.
les ions ${\rm Cl}^-$ sont consommés, la concentration des ions ${\rm Cl}^-$ diminue.
Les ions K+, présents dans la solution, ne réagissent pas : la concentration des ions K+ ne varie pas.
| Ions | Avant l’équivalence |
| Ag+ | 0 |
| NO3– | ↗ |
| Cl– | ↘ |
| K+ | = |
Donc les ions ${\rm Cl}^-$ sont remplacés par des ions ${\rm NO}3^-$
Or $\lambda{{\rm Cl}^-}>\lambda_{{\rm NO}_3^-\ }$ ainsi $\mathbf{\sigma}$ diminue avant l’équivalence.
Après l’équivalence :
les ions ${\rm Ag}^+$sont ajoutés et ne sont plus consommés, la concentration des ions ${\rm Ag}^+$augmente.
les ions ${\rm NO}_3^-$ sont ajoutés, ils ne réagissent pas, la concentration des ions ${\rm NO}_3^-$ augmente.
les ions ${\rm Cl}^-$ n’existent plus, la concentration des ions ${\rm Cl}^-$ est nulle.
Les ions K+, présents dans la solution, ne réagissent pas : la concentration des ions K+ ne varie pas.
| Ions | Après l’équivalence |
| Ag+ | ↗ |
| NO3– | ↗ |
| Cl– | 0 |
| K+ | = |
La concentration des ions augmente, ainsi $\mathbf{\sigma}$ augmente après l’équivalence.
