Bac Polynésie septembre 2023
Exercice 3 – (4 points) – Durée 0h42 – Calculatrice autorisée
Sujet n°23-PYCJ1PO3
Sujet et corrigé
EXERCICE 3 – ÉTUDE D’UN TRAITEMENT CONTRE LES VERRUES (4 points).
Afin d’éliminer les verrues simples, lésions cutanées d’origine virale très contagieuses et souvent douloureuses, il est coutume de les « brûler ». Un traitement par le froid ou une brûlure chimique ont l’effet identique de déshydrater les cellules contaminées et de provoquer la destruction du virus. Les lésions peuvent ainsi guérir et la peau cicatriser. Il est possible de se procurer en pharmacie des crayons qui permettent, à la maison, de traiter sélectivement la verrue. Certains, qui provoquent une brûlure chimique, contiennent une solution gélifiée d’acide trichloroacétique à 40,0% en masse.
L’objectif de cet exercice est de vérifier la concentration en quantité de matière d’acide trichloroacétique du crayon utilisé pour traiter les verrues.
Données :
- couple acide trichloroacétique/ion trichloroacétate: C2HO2Cl3(aq) /C2O2Cl3–(aq) ;
- masse volumique ρ de la solution à 40,0% en masse d’acide trichloroacétique : ρ = 1,50×103 g·L–1 ;
- masse molaire moléculaire de l’acide trichloroacétique : M = 163,5 g·mol–1.
On souhaite préparer un volume V de valeur égale à 100,0 mL d’une solution S0 d’acide trichloroacétique à 40,0% en masse.
Q1. Calculer la valeur de la masse m d’acide trichloroacétique à peser pour préparer cette solution S0.
$$P_{acide\ trichloroacetique}=\frac{m_{acide\ trichloroacetique}}{m_{solution}}$$
$$\frac{m_{acide\ trichloroacetique}}{m_{solution}}=P_{acide\ trichloroacetique}$$
$$m_{acide\ trichloroacetique}=P_{acide\ trichloroacetique}\times m_{solution}$$
Or
$$\rho_{solution}=\frac{m_{solution}}{V_{sol}}$$
$$\frac{m_{solution}}{V_{sol}}=\rho_{solution}$$
$$m_{solution}=\rho_{solution}\times V_{sol}$$
D’où
$$m_{acide\ trichloroacetique}=P_{acide\ trichloroacetique}\times \rho_{solution}\times V_{sol}$$
$$m_{acide\ trichloroacetique}=\frac{40}{100}\times 1,50\times{10}^3\times 100\times{10}^{-3}$$
$$m_{acide\ trichloroacetique}=60\ g$$
Pour préparer cette solution S0, il faut peser une masse m=60 g d’acide trichloroacétique.
Q2. Vérifier que la valeur de la concentration en quantité de matière c0 de la solution S0 d’acide trichloroacétique ainsi préparée, est égale à 3,67 mol·L–1.
$$c_0=\frac{n}{V}$$
Or
$$n=\frac{m}{M}$$
D’où
$$c_0=\frac{\frac{m}{M}}{V}$$
$$c_0=\frac{m}{M\times V}$$
$$c_0=\frac{60}{163,5\times 100\times{10}^{-3}}$$
$$c_0=3,67\ mol{.L}^{-1}$$
On réalise une dilution au centième de la solution S0. Cette solution diluée est notée S1. Un volume V1 = 20,0 mL de la solution S1 est dosé par une solution aqueuse d’hydroxyde de sodium (Na+(aq) + HO–(aq)) de concentration c2 = 5,00×10–2 mol·L–1.
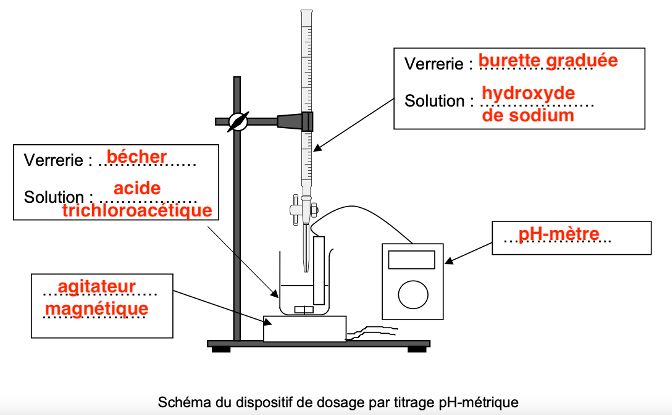
Q3. Sur le document réponse à rendre obligatoirement avec la copie, annoter le schéma du dispositif utilisé pour le dosage pH-métrique réalisé.
La courbe de la figure 1 représente le suivi pH-métrique du milieu réactionnel.
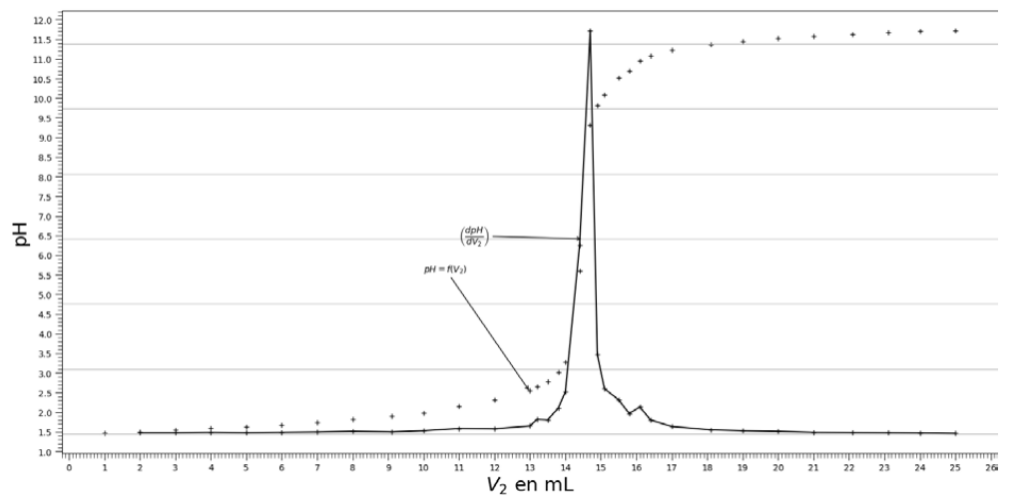
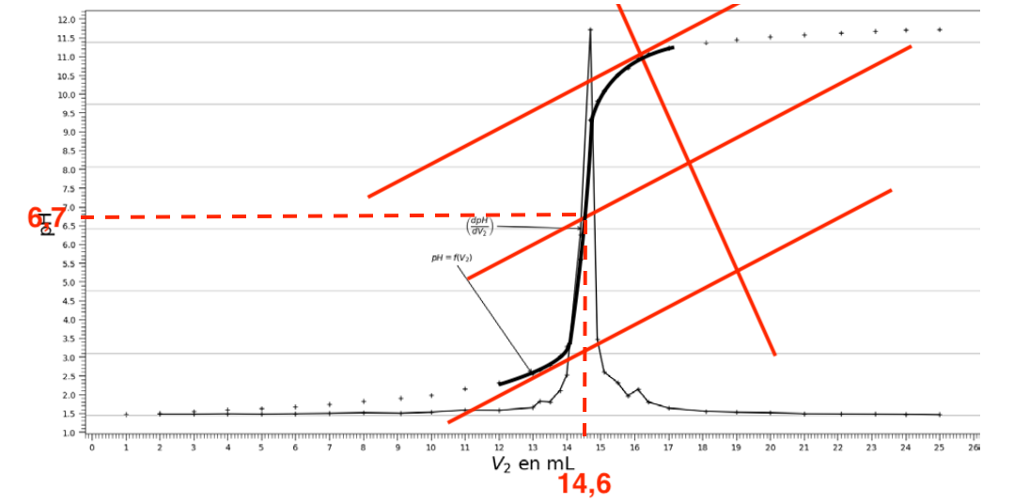
Figure 1. Courbe du dosage de la solution S1 par la solution d’hydroxyde de sodium de concentration en quantité de matière c2
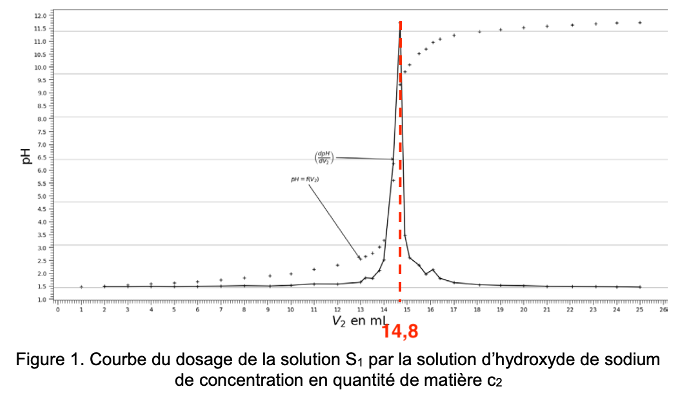
Q4. À l’aide de la courbe de la figure 1, déterminer le volume V2E de solution d’hydroxyde sodium versé à l’équivalence. Nommer la méthode utilisée.
On détermine graphiquement $V_{2E}$ qui se repère au maximum de la courbe $\frac{dpH}{dV}$ :
$$V_{2E}=14,8\ mL$$
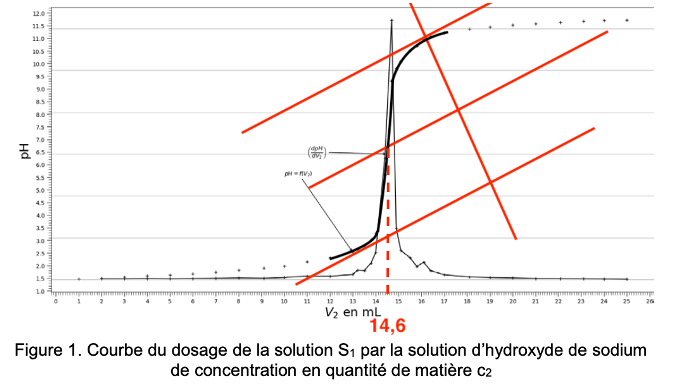
On peut aussi utiliser la méthode des tangentes parallèles :
On trouve $V_{2E}=14,6\ mL$
On veut modéliser la transformation chimique observée lors de la réalisation du dosage par l’hydroxyde de sodium en solution. L’acide trichloroacétique sera noté AH, tandis que l’ion trichloroacétate sera noté A–.
Q5. Écrire l’équation de la réaction modélisant la transformation observée durant le dosage.
$${\rm AH}{(aq)}\ +\ HO{(aq)}^-\ \ \rightarrow A_{(aq)}^-+\ H_2O_{(\ell)}$$
Q6. Déterminer la valeur de la concentration en quantité de matière c1 de la solution diluée d’acide trichloroacétique S1.
A l’équivalence :
$$\frac{n_{AH}^i}{1}=\frac{n_{HO^-}^{eq}}{1}$$
$$c_1V_1=C_2V_{2E}$$
$$c_1=\frac{C_2V_{2E}\ }{V_1}$$
$$c_1=\frac{5,00{\times10}^{-2}\times 14,8{\times10}^{-3}}{20,0{\times10}^{-3}}$$
$$c_1=3,70{\times10}^{-2}\ mol{.L}^{-1}$$
Q7. En déduire la valeur de la concentration en quantité de matière c0exp de la solution aqueuse d’acide trichloroacétique S0.
D’après l’énoncé : « On réalise une dilution au centième de la solution S0. Cette solution diluée est notée S1.»
$$F=\frac{c_{0exp}}{c_1}$$
$$\frac{c_{0exp}}{c_1}=F$$
$$c_{0exp}=F\times c_1$$
$$c_{0exp}=100\times 3,70{\times10}^{-2}$$
$$c_{0exp}=3,70\ mol{.L}^{-1}$$
On note u(c0exp) l’incertitude-type sur la valeur de la concentration c0exp de la solution S0. Une simulation via l’exécution d’un programme Python donne la valeur de u(c0exp) égale à 4×10-2 mol·L–1.
Donnée :
Le résultat d’une mesure est en accord avec une valeur de référence si la valeur du quotient $\frac{\left|x-x_{ref}\right|}{u(x)}$ est inférieure ou égale à 2, avec :
- x, la valeur expérimentale,
- xref, la valeur de référence,
- u(x), l’incertitude-type.
Q8. Vérifier la compatibilité de la valeur de c0exp trouvée à l’issu du dosage à celle de la valeur de référence c0 de la question Q2.
$$\frac{\left|x-x_{ref}\right|}{u(x)}$$
$$\frac{\left|c_{0exp}-c_0\right|}{u\left(c_{0exp}\right)}$$
$$\frac{\left|c_{0exp}-c_0\right|}{u\left(c_{0exp}\right)}=\frac{\left|3,70-3,67\right|}{4{\times10}^{-2}}$$
$$\frac{\left|c_{0exp}-c_0\right|}{u\left(c_{0exp}\right)}=0,75$$
$\frac{\left|c_{0exp}-c_0\right|}{u\left(c_{0exp}\right)}<2$ , $c_{0exp}$ et $c_0$ sont compatibles.
Pour mettre en place un contrôle-qualité rapide et plus systématique, on souhaite remplacer l’usage du pH-mètre dans le dosage par l’emploi d’un simple indicateur coloré acido-basique.
| Indicateur coloré | zone de virage | pKa | forme acide | forme basique |
| Bleu de thymol | 1,2 à 2,8 | 1,6 | rouge | jaune |
| Rouge de phénol | 6,0 à 8,0 | 7,1 | jaune | rouge |
| Thymolphtaléine | 9,3 à 10,5 | 9,9 | incolore | bleu |
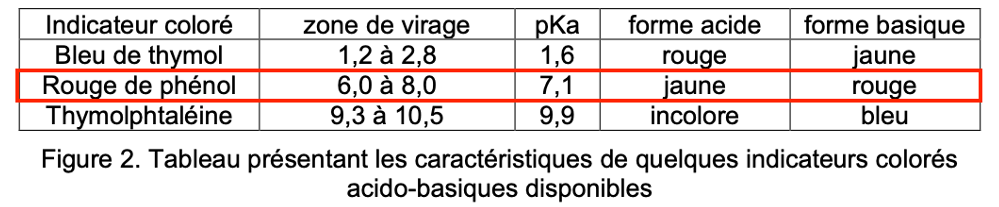
Figure 2. Tableau présentant les caractéristiques de quelques indicateurs colorés acido-basiques disponibles
Q9. À partir de la figure 2, choisir l’indicateur coloré le plus pertinent pour le dosage de l’acide trichloroacétique parmi le choix proposé. Justifier la réponse.
Pour choisir un indicateur coloré, sa zone de virage doit contenir le pHeq du point équivalent.
Graphiquement $pHeq=6,7$
Le rouge de phénol contient 6,7 dans sa zone de virage.
Le rouge de phénol est l’indicateur coloré le plus pertinent pour le dosage de l’acide trichloroacétique.
EXERCICE 3 – ÉTUDE D’UN TRAITEMENT CONTRE LES VERRUES
Q3. Annoter le schéma du dispositif utilisé pour le dosage pH-métrique réalisé.
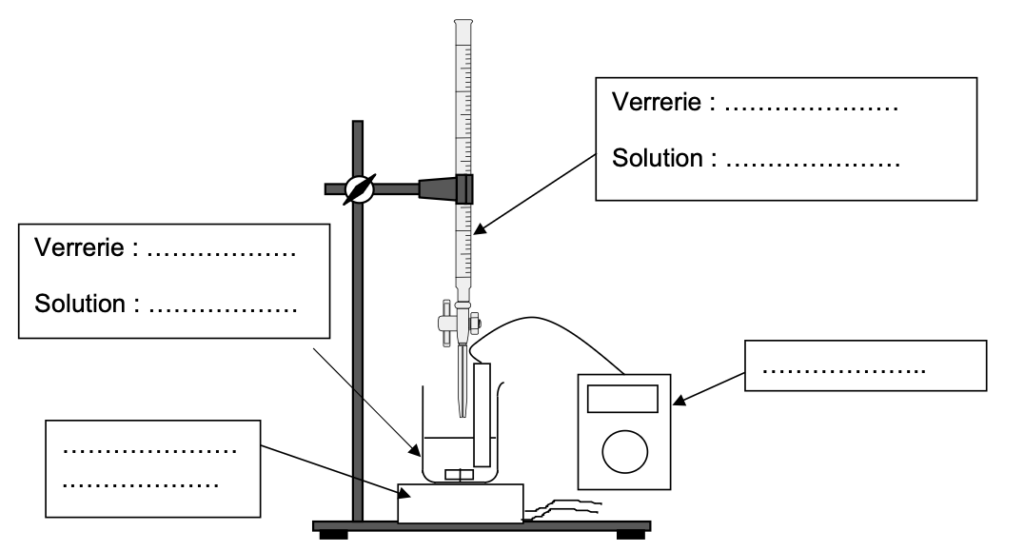
Schéma du dispositif de dosage par titrage pH-métrique
