Bac Polynésie 2023 Sujet 1
Exercice 1 – (9 points) – Durée 1h35 – Calculatrice autorisée
Sujet n°23-PYCJ1PO1
Sujet et corrigé
EXERCICE 1 – AUTOUR DE LA BIOSYNTHÈSE DE LA MÉLANINE (9 points)
Le terme « mélanine » regroupe un ensemble de pigments présents chez la plupart des êtres vivants. La mélanine est responsable de la coloration de la peau, des poils et des yeux chez tous les mammifères, mais se retrouve également dans les plumes des oiseaux, les ailes de certains papillons et même chez les champignons.
Il existe deux grands types de mélanines biologiques : l’eumélanine brune et la phéomélanine rouge. L’eumélanine est synthétisée dans les cellules à partir de tyrosinase grâce à l’enzyme tyrosinase.
L’objectif de cet exercice est l’étude du suivi de la synthèse de l’eumélanine assistée par de la tyrosinase extraite de champignons de Paris.
Étude des formes acide-base de la tyrosine.
En solution, la tyrosine existe sous quatre formes acide/base dont l’une est représentée figure 1.
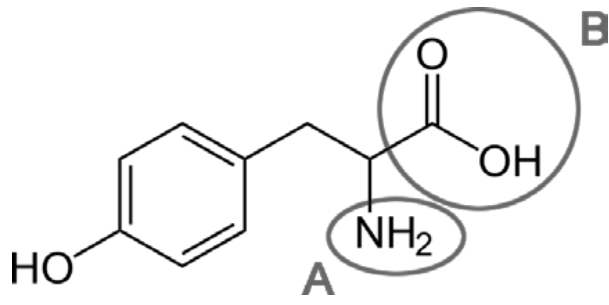
Figure 1. Représentation de l’une des formes de la tyrosine.
Q1. Indiquer le type de représentation de la tyrosine présente sur la figure 1.
Le type de représentation de la tyrosine présente sur la figure 1 est une représentation topologique.
Q2. Nommer les familles fonctionnelles associées aux groupes caractéristiques A et B mis en évidence dans la représentation de la forme de la tyrosine figure 1.
Les familles fonctionnelles associées aux groupes caractéristiques A et B mis en évidence dans la représentation de la forme de la tyrosine figure 1 sont
A : amine
B : Acide carboxylique
Le tableau de la figure 2 représente les quatre formes de la tyrosine.
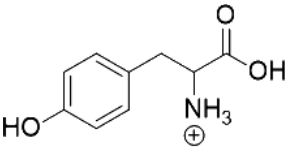 | 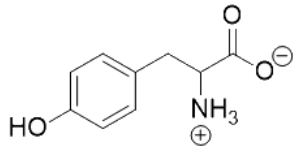 | 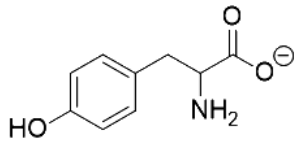 | 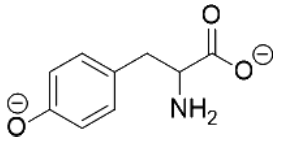 |
| TyrH3+ | TyrH2 | TyrH– | Tyr2– |
Figure 2. Tableau récapitulatif des quatre formes de la tyrosine.
Données :
- La valeur du pKA(TyrH3+/TyrH2) du couple TyrH3+/TyrH2 est égale à 2,20.
- La valeur du pKA(TyrH2/TyrH –) du couple TyrH2TyrH – est égale à 9,11.
- La valeur du pKA(TyrH –/Tyr 2–) du couple TyrH –/Tyr 2– est égale à 10,07
Q3. Tracer le diagramme de prédominance des quatre formes associées à la tyrosine.
Diagramme de prédominance :
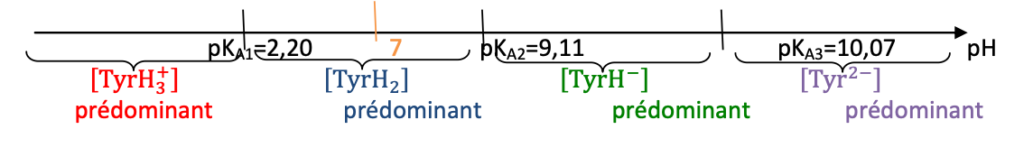
Q4. Déterminer la forme de la tyrosine prédominante dans une solution dont la valeur du pH est égale à 7.
La forme de la tyrosine prédominante dans une solution dont la valeur du pH est égale à 7 est TyrH2.
Synthèse in vitro de la mélanine.
La synthèse au laboratoire de la mélanine se déroule comme suit :
- Une solution d’enzyme tyrosinase est obtenue par broyage de pieds de champignons de Paris puis filtration.
- Dans un tube à essais, introduire un volume Vtyr de solution de tyrosine de valeur égale à 3,0 mL de concentration en quantité de matière ctyr de valeur égale à 2,6×10–3 mol·L–1 et un volume de filtrat Vfiltrat de valeur égale à 2,0 mL.
- L’évolution de la coloration de la solution contenue dans le tube à essais, due à la transformation totale de la tyrosine en un premier intermédiaire appelé DOPAchrome, est suivi par spectrophotométrie.
- Si on prolonge l’expérimentation, environ 24 heures, des eumélanines noires insolubles précipitent.
La tyrosinase permet d’accélérer la réaction de synthèse sans pour autant modifier le bilan de matière.
Q5. Nommer le rôle joué par la tyrosinase.
La tyrosinase permet d’accélérer la réaction de synthèse sans pour autant modifier le bilan de matière : la tyrosinase joue le rôle de catalyseur.
Q6. Proposer une technique de séparation permettant de récupérer les molécules d’eumélanines insolubles présentes à la fin de la réaction en citant le matériel nécessaire.
Les molécules d’eumélanines sont insolubles : on peut les récupérer par filtration.
Matériel nécessaire à la filtration :
Un entonnoir
Un papier filtre
Un erlenmeyer
Suivi spectrophotométrique de la synthèse.
On s’intéresse à la première étape de la synthèse, correspondant à la formation de DOPAchrome.
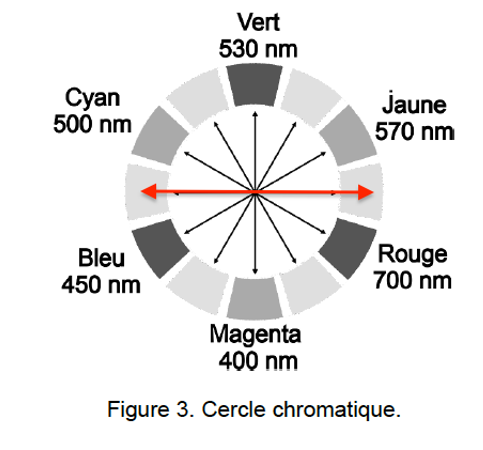
On représente le cercle chromatique en figure 3.
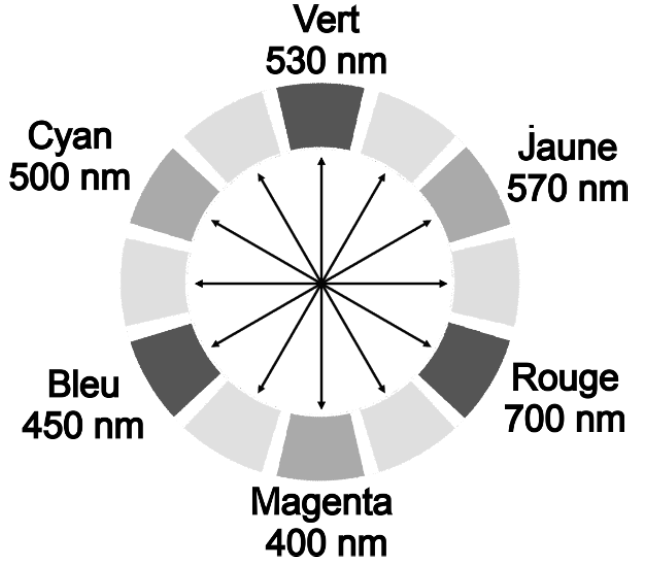
Figure 3. Cercle chromatique.
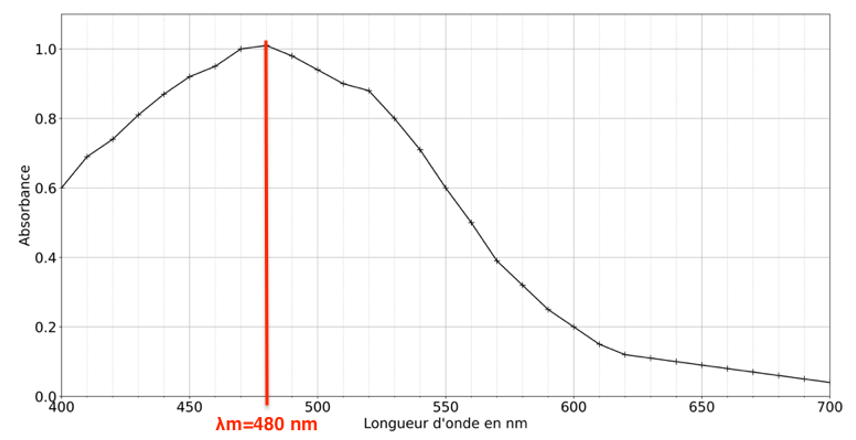
La figure 4 représente le spectre d’absorption de la molécule de DOPAchrome.
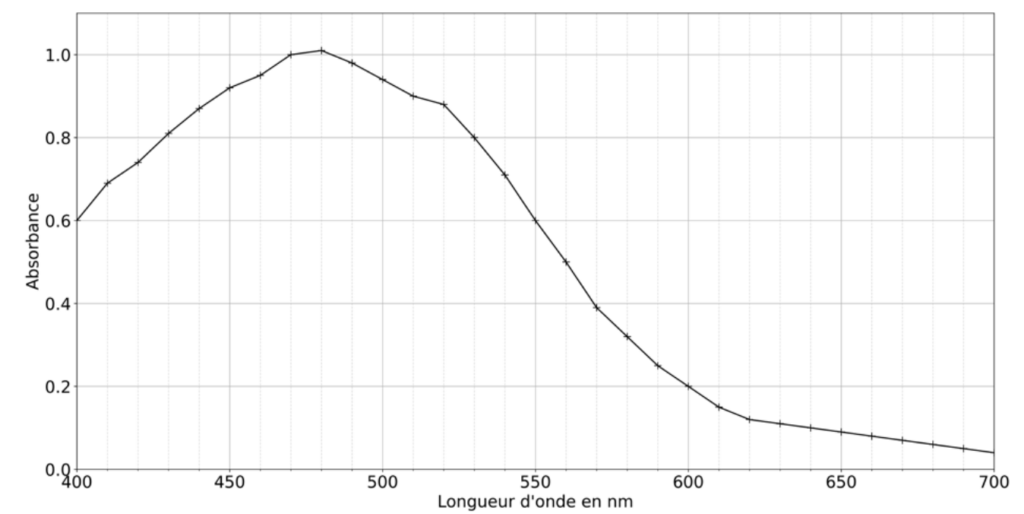
Figure 4. Spectre d’absorption de la molécule DOPAchrome.
Q7. À l’aide de la figure 4, indiquer la longueur d’onde λm la plus adaptée au suivi spectrophotométrique.
On choisit la longueur d’onde correspondante au maximum de l’absorbance :
$$\lambda_m=480\ nm$$
Q8. À l’aide des figures 3 et 4, déterminer la couleur de la molécule DOPAchrome.
$\lambda_m=480\ nm$ : la couleur absorbée est entre le bleu et le cyan.
La couleur de la molécule DOPAchrome est la couleur complémentaire. La couleur complémentaire est celle opposée sur le cercle chromatique.
La couleur de la molécule DOPAchrome est le orange (entre le jaune et le rouge).
Le suivi spectrophotométrique de la réaction de formation de DOPAchrome à la longueur d’onde λm est représenté figure 5.
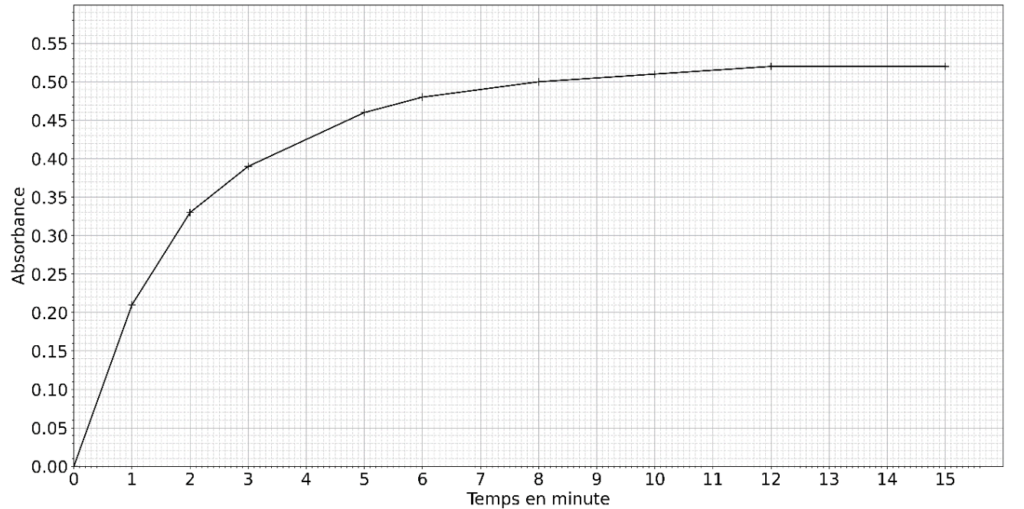
Figure 5. Suivi spectrophotométrique de la réaction de formation de DOPAchrome.
Q9. Exprimer la loi de Beer-Lambert reliant l’absorbance A de la solution et la concentration en espèce chimique formée cDOPA.
Loi de Beer-Lambert :
$$A=k\left[DOPAchrome\right]$$
Q10. Expliquer pourquoi l’absorbance A de la solution augmente au cours de cette réaction.
$$A=k\left[DOPAchrome\right]$$
A est proportionnel à la concentration de la DOPAchrome. Or la DOPAchrome est un produit de la réaction : sa concentration augmente au cours de la réaction.
Ainsi, l’absorbance A de la solution augmente au cours de cette réaction.
Pour la question suivante, le candidat est invité à prendre des initiatives et à présenter la démarche suivie, même si elle n’a pas abouti. La démarche est évaluée et nécessite d’être correctement présentée.
Donnée :
Le coefficient de proportionnalité de la loi de Beer-Lambert pour le dosage de la DOPAchrome à la longueur d’onde λm possède une valeur égale à 3,6×103 L·mol–1.
Q11. Exprimer puis calculer la valeur de la quantité en DOPAchrome nDOPA formée à l’issue de la réaction suivie figure 5.
$$n_{DOPAchrome}=\left[DOPAchrome\right]\times V$$
Or
$$A=k\left[DOPAchrome\right]$$
$$\left[DOPAchrome\right]=\frac{A}{k}$$
D’ou
$$n_{DOPAchrome}=\frac{A}{k}\times V$$
Le volume V est le volume de la solution soit :
$$V=V_{tyr}+V_{filtrat}$$
D’ou
$$n_{DOPAchrome}=\frac{A}{k}\times\left(V_{tyr}+V_{filtrat}\right)$$
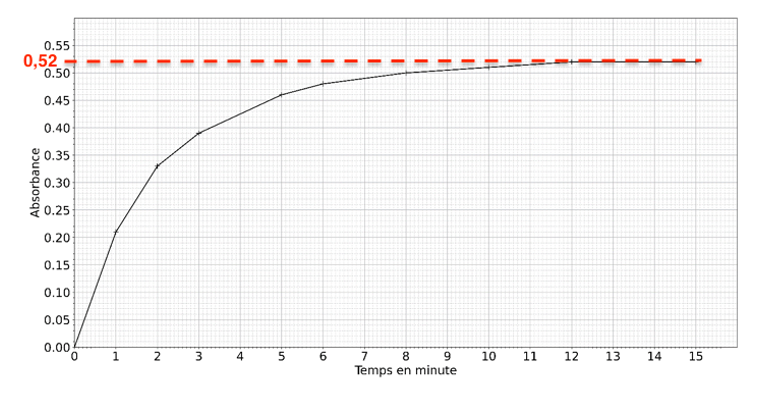
Graphiquement, a l’issue de la réaction suivie figure 5 : $A=0,52$
$$n_{DOPAchrome}=\frac{0,52}{3,6\times {10}^3}\times\left(3,0\times {10}^{-3}+2,0\times {10}^{-3}\right)$$
$$n_{DOPAchrome}=7,2\times {10}^{-7}\ mol$$
On considère qu’à l’issue de la réaction suivie figure 5, une quantité de matière de DOPAchrome nD de valeur égale à 7,2×10–7 mol s’est formée pour une quantité de matière de tyrosine nT de valeur égale à 7,8×10–6 mol.
Données :
- Masse molaire MDOPA de la DOPAchrome : MDOPA = 193 g·mol–1 ;
- Masse molaire MTde la tyrosine : MT = 181 g·mol–1.
Q12. Déterminer la masse de tyrosine m’tyr nécessaire à la synthèse d’une masse m’DOPA égale à 1,0 mg de DOPAchrome.
$${n\prime}{DOPAchrome}=\frac{{m\prime}{DOPAchrome}}{M_{DOPAchrome}}$$
$${n\prime}_{DOPAchrome}=\frac{1,0\times {10}^{-3}}{193}=5,2\times {10}^{-6}mol$$
| DOPAchrome | tyrosine |
| $n_D=7,2\times {10}^{-7}mol$ | $n_T=7,8\times {10}^{-6}mol$ |
| ${n^\prime}_{DOPAchrome}=5,2\times {10}^{-6}mol$ | ${n^\prime}_{tyrosine}$ |
$${n^\prime}_{tyrosine}=\frac{5,2\times {10}^{-6}\times 7,8\times {10}^{-6}}{7,2\times {10}^{-7}}$$
$${n^\prime}_{tyrosine}=5,6\times {10}^{-5}\ mol$$
$${n^\prime}_{tyrosine}=\frac{{m^\prime}_{tyrosine}}{M_{tyrosine}}$$
$${m^\prime}_{tyrosine}={n^\prime}_{tyrosine}\times M_{tyrosine}$$
$${m^\prime}_{tyrosine}=5,6\times {10}^{-5}\ \times 181$$
$${m^\prime}_{tyrosine}=1,0\times {10}^{-2}\ \ g$$
$${m^\prime}_{tyrosine}=10\ mg$$
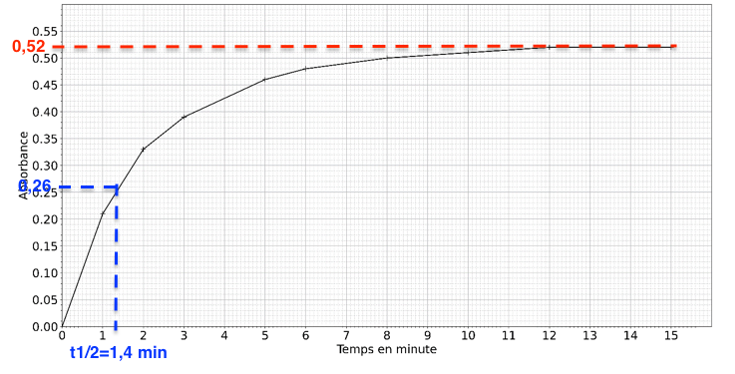
Q13. À l’aide de la figure 5, déterminer la valeur du temps de demi-réaction t1/2.
$t_{1/2}$ est la durée nécessaire pour que l’avancement atteigne la moitié de sa valeur finale : $x(t_{1/2})=x_f/2$.
$A(t_{1/2})=A_f/2$
$A(t_{1/2})=0,52/2$
$A(t_{1/2})=0,26$
Par lecture graphique : $t_{1/2}=1,4\ min$.
Q14. Indiquer comment évolue la vitesse volumique de réaction au cours du temps, et expliquer cette variation.
$$v_{DOPAchrome}=\frac{d\left[DOPAchrome\right]}{dt}$$
Or
$$A=k\left[DOPAchrome\right]$$
$$\left[DOPAchrome\right]=\frac{A}{k}$$
$$v_{DOPAchrome}=\frac{d\frac{A}{k}}{dt}$$
$$v_{DOPAchrome}=\frac{1}{k}\frac{dA}{dt}$$
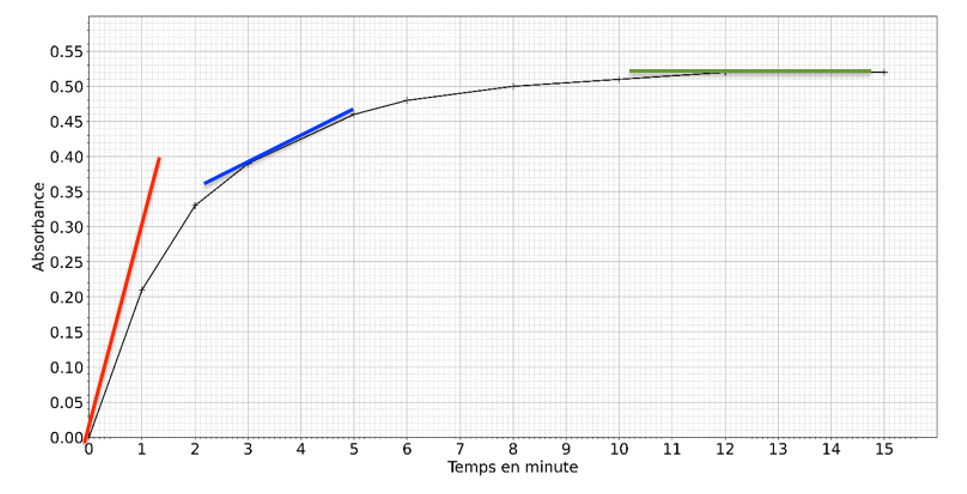
La dérivée se calcul en trouvant le coefficient directeur de la tangente en un point de la courbe.
La pente décroit au cours du temps. Ainsi la vitesse volumique de réaction, diminue au cours du temps.
Au cours de la réaction, les réactifs sont consommés, leur concentration diminue. Or la concentration des réactifs est un facteur cinétique. Comme la concentration des réactifs diminue, la vitesse diminue au cours de la réaction.
On effectue la même expérience à partir d’une autre solution obtenue par dilution de la solution de tyrosine utilisée précédemment.
Q15. Comparer qualitativement la vitesse volumique initiale au cours de cette expérience à celle obtenue lors de l’expérience précédente.
La concentration des réactifs est un facteur cinétique.
Avec la dilution, la concentration des réactifs sera plus faible que dans l’expérience précédente : la vitesse volumique initiale au cours de cette expérience sera plus faible que celle obtenue lors de l’expérience précédente.
