Bac Liban 2024 Sujet 1
Exercice 1 – (9 points) – Durée 1h35 – Calculatrice autorisée
Sujet n°24-PYCJ1G11
Sujet et corrigé
EXERCICE 1 : certification d’un vin (9 points)
Le vin est une boisson alcoolisée obtenue par la fermentation du raisin et qui doit avoir un titre massique de 8,5 % d’alcool au minimum. Dans le cas de la composition du vin, il y a plus de 600 substances différentes mais l’espèce chimique majoritaire est l’eau. On y trouve également de l’éthanol, de l’éthanal et d’autres composés aromatiques issus de la fermentation qui participent à l’arôme des vins jeunes.
Les démarches de certifications environnementales sont nombreuses en viticulture. Parmi celles- ci, on peut citer le label agriculture biologique (AB), la certification Terra Vitis, ou encore le label Demeter. Un des critères à respecter pour obtenir ces labels concerne le taux de dioxyde de soufre total présent dans le vin.
Selon : shop.abacchus.fr/blog-vin/composition-du-vin-les-600-substances/
Règles de nomenclature dans le cas de composés à chaîne non ramifiée :
| Nombre d’atomes de carbone | 1 | 2 | 3 | 4 | 5 |
| Préfixe du nom de la chaine carbonée | méth… | éth… | prop… | but… | pent… |
| Fonction | Groupe caractéristique | Nomenclature du groupe caractéristique |
| Acide carboxylique | 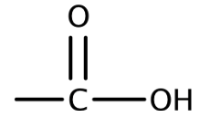 | acide …oïque |
| Ester | 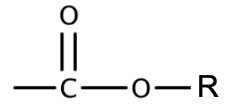 | …oate de …yle |
| Aldéhyde | 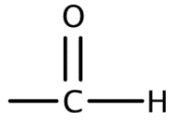 | …al |
1. Composition d’un vin
Q.1. Écrire la formule semi-développée de l’éthanal.
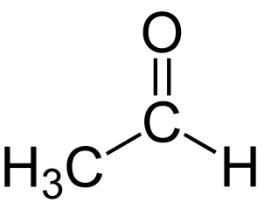
La formule topologique d’une espèce chimique qui participe à l’arome du vin, autre que l’éthanal, est donnée ci-dessous :
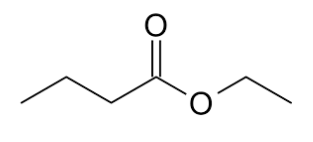
Q.2. Écrire la formule semi-développée de cette molécule. Entourer le groupe caractéristique présent dans cette molécule et nommer la famille fonctionnelle associée.
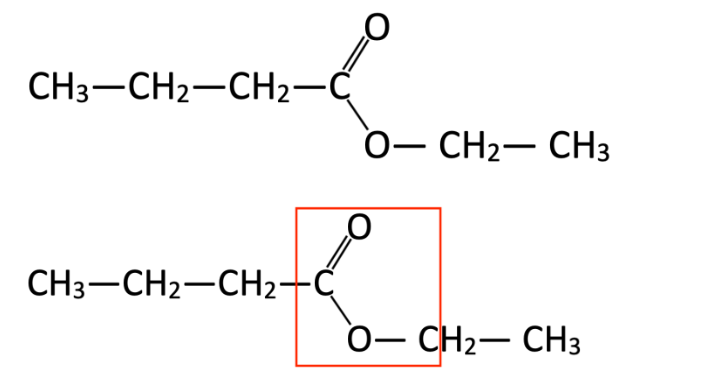
Famille fonctionnelle associée : Ester
Q.3. Nommer cette molécule.
Butanoate d’éthyle.
2. Différentes formes prises par le dioxyde de soufre dans le vin
La plupart des vignerons introduisent du dioxyde de soufre dans le vin. Le dioxyde de soufre agit comme antiseptique, antioxydant et régulateur de fermentation. Les vignerons peuvent l’ajouter de différentes manières mais cela revient, au final, à libérer dans la solution du (SO2,H2O) également noté (H2SO3(aq)).
Données :
– pKA1(H2SO3(aq) / HSO3–(aq)) = 1,8 ;
– pKA2 (HSO3–(aq) / SO32-(aq)) = 7,2.
Q.4. Écrire l’équation de la réaction modélisant la transformation de l’acide sulfureux H2SO3(aq), avec l’eau.
$$H_2SO_3\left(aq\right)+H_2O\left(l\right)\rightarrow HSO_3^-\left(aq\right)+H_3O^+\left(aq\right)$$
Q.5. Exprimer la constante d’acidité KA1 associée à cette équation de réaction.
$$K_A=\frac{[A^-]{eq}\times[H_3O^+]{eq}}{[HA]{eq}\times c_0}$$
$$K{A1}=\frac{[HSO_3^-]{eq}\times[H_3O^+]{eq}}{[H_2SO_3]_{eq}\times c_0}$$
Q.6. Justifier le caractère amphotère de l’espèce chimique HSO3–(aq).
L’espèce chimique $HSO_3^-$ est la base du couple : $H_2SO_3\left(aq\right)/HSO_3^-\left(aq\right)$
L’espèce chimique $HSO_3^-$ est l’acide du couple : $HSO_3^-\left(aq\right)/SO_3^{2-}\left(aq\right)$
Ainsi, l’espèce chimique $HSO_3^-$ est amphotère.
Q.7. Représenter le diagramme de prédominance pour les trois espèces contenant l’élément soufre.
Diagramme de prédominance :
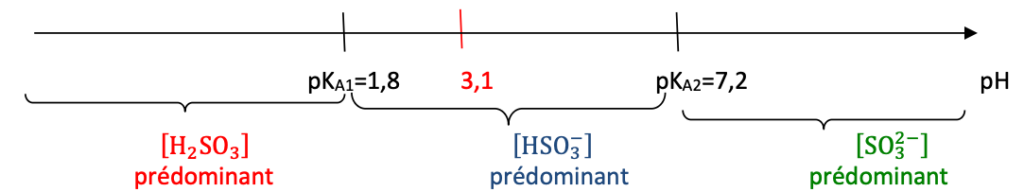
Q.8. Indiquer l’espèce soufrée prédominante contenue dans un vin dont le pH vaut 3,1. Justifier.
D’après le diagramme de prédominance, pour un vin dont le pH vaut 3,1, l’espèce soufrée prédominante est $HSO_3^-$.
3. Titrage colorimétrique du dioxyde de soufre total par une solution de diiode
Pour titrer le dioxyde de soufre dissous, on utilise une solution de diiode. La solution de diiode étant peu stable, il faut vérifier sa concentration en quantité de matière de I2 en effectuant un dosage par étalonnage utilisant des mesures d’absorbance.
Partie 1 : vérification de la concentration de la solution titrante
La solution disponible étant trop concentrée, on la dilue 10 fois. On note S1 la solution diluée.
Q.9. Décrire le protocole de dilution pour préparer 100,0 mL de solution diluée de diiode en précisant la verrerie utilisée.
On souhaite diluer 10 fois, ainsi le facteur de dilution est 10 : le volume de la solution fille est 10 fois plus grand que le volume de la solution mère.
Protocole expérimental :
On prélève le volume $V_m=10,0\ mL$ à l’aide d’une pipette jaugée de 10,0 mL
On introduit $V_m=10,0\ mL$ dans une fiole jaugée de volume $V_f=100,0\ mL$
On complète aoverrightarrow de l’eau distillée jusqu’au trait de jauge et on homogénéise.
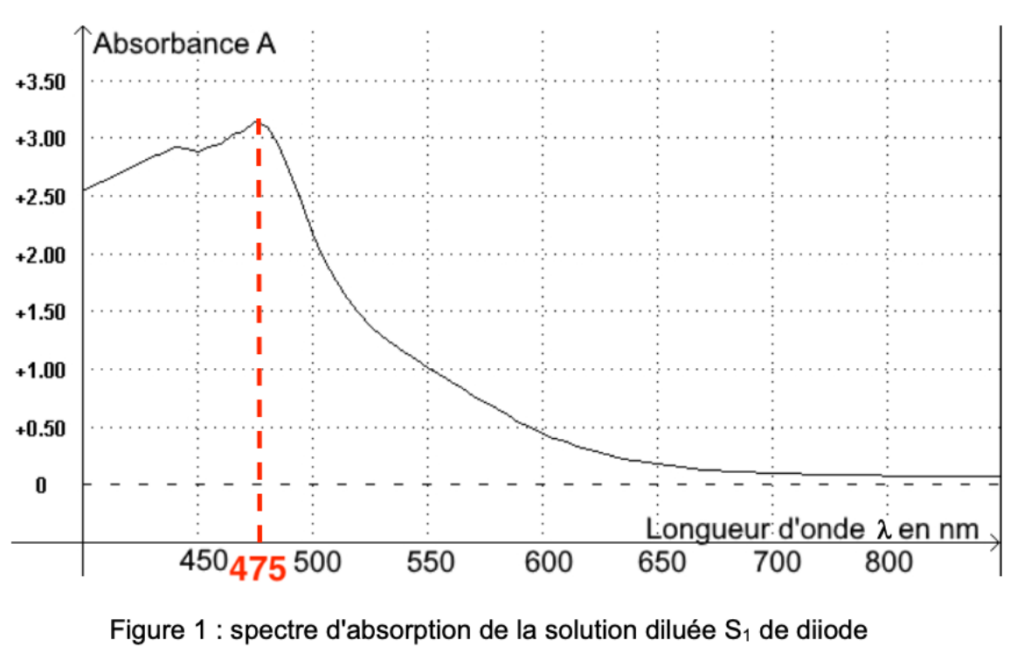
Le spectre d’absorption de la solution diluée S1 de diiode est le suivant :
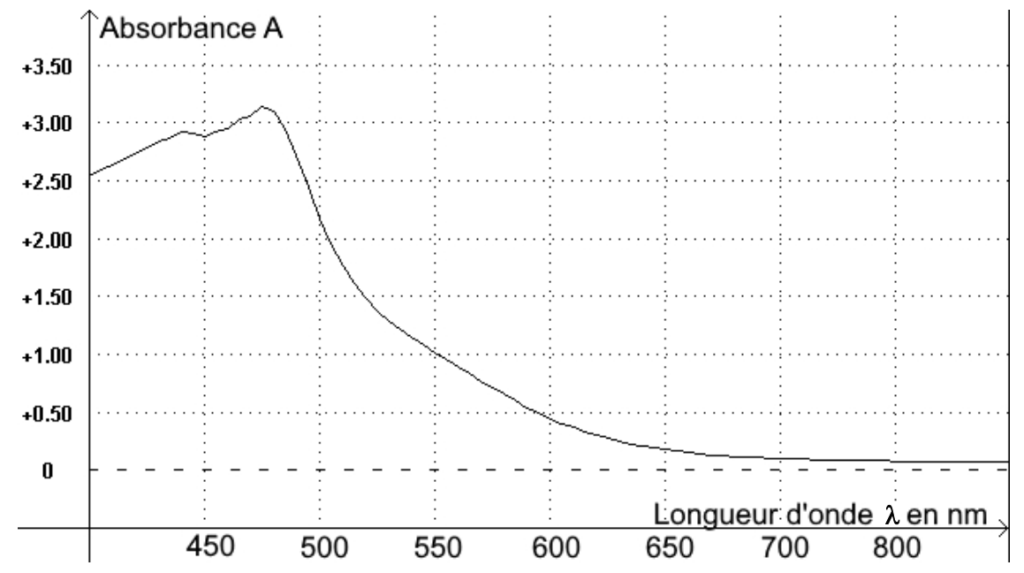
Figure 1 : spectre d’absorption de la solution diluée S1 de diiode
Q.10. Déterminer la longueur d’onde pertinente pour laquelle les mesures d’absorbance seront réalisées en exploitant la figure 1. Justifier le choix.
La longueur d’onde pertinente pour laquelle les mesures d’absorbance seront réalisées est celle pour laquelle l’absorbance est maximale : $\lambda_{max}=475\ nm$
À partir de S1, on prépare cinq solutions étalons de diiode. On mesure l’absorbance de ces cinq solutions et on trace l’évolution de l’absorbance en fonction de la concentration en diiode.
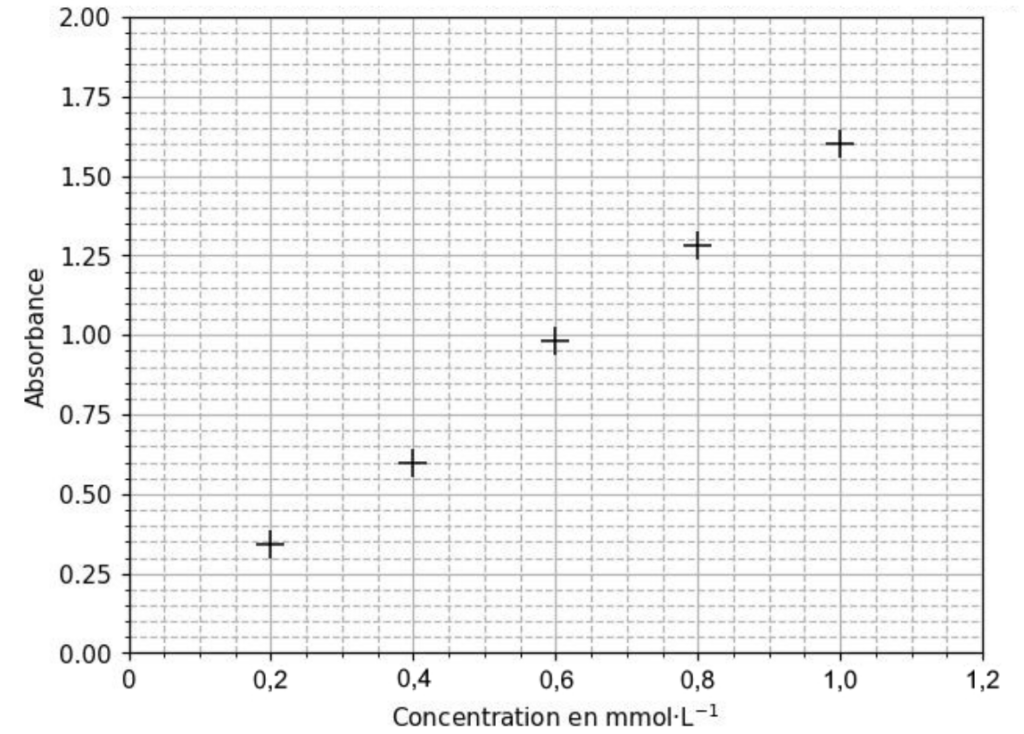
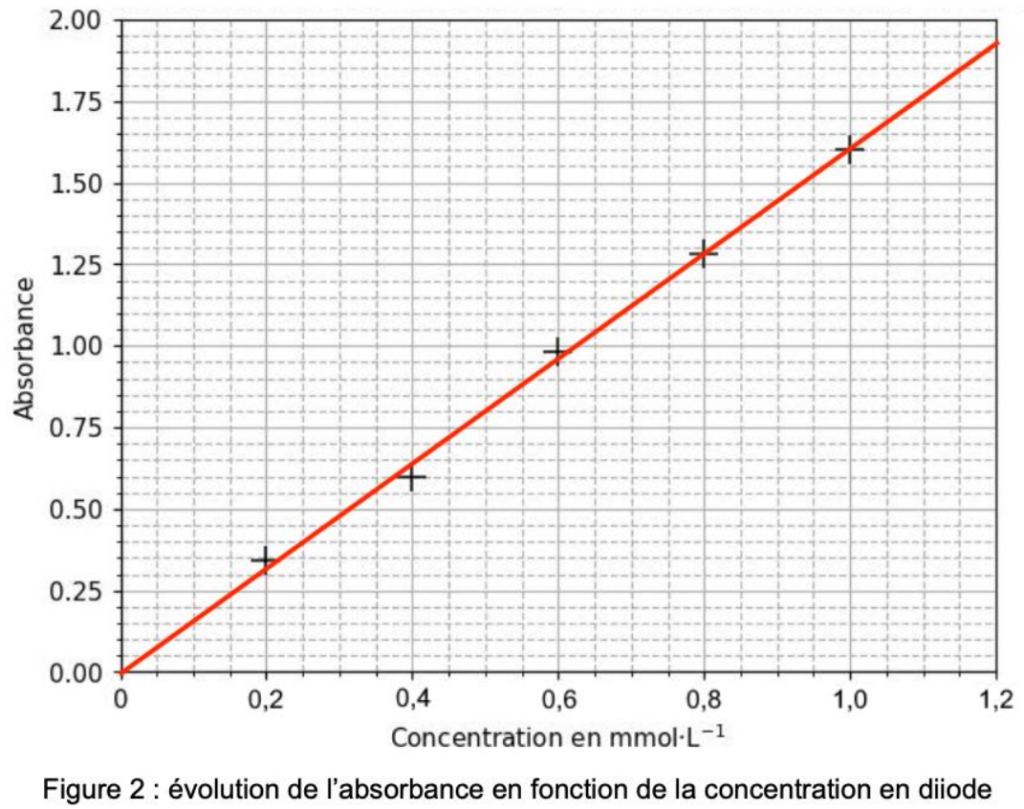
Figure 2 : évolution de l’absorbance en fonction de la concentration en diiode
Q.11. Montrer que les mesures obtenues pour les solutions étalons de diiode peuvent être modélisées par la loi de Beer-Lambert.
L’évolution de l’absorbance en fonction de la concentration en diiode peut être modélisée par une droite passant par l’origine.
Ainsi l’absorbance $A$ est proportionnelle à $C$ : $A=K\times C$.
Les solutions étalons de diiode peuvent donc être modélisées par la loi de Beer-Lambert.
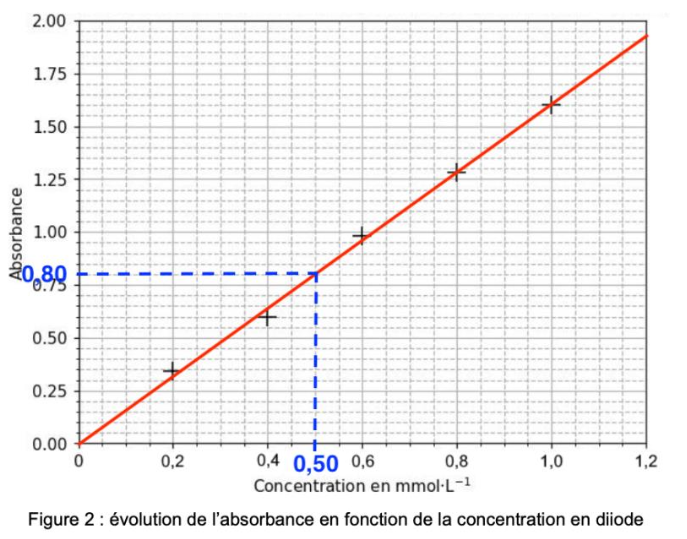
On mesure la valeur de l’absorbance de la solution titrante de diiode S1 à la longueur d’onde déterminée à la Q.10 : A1 = 0,80.
Q.12. Déterminer la valeur de la concentration en quantité de matière de diiode de la solution S1.
Graphiquement, pour $A_1=0,80$, $C_1=0,50\ mmol.L^{-1}$.
Partie 2 : titrage colorimétrique du dioxyde de soufre total
Données :
- couples oxydant/réducteur SO4 2-(aq) / H2SO3(aq) ; I2(aq) / I–(aq) ;
- masse molaire H2SO3 : M = 82,1 g·mol-1 ;
- critères à respecter concernant le taux de dioxyde de soufre total présent dans le vin pour différents labels :
| Certification | AB | Terra Vitis | Demeter |
| Concentration en masse maximale de SO2,H2O totale (mg·L-1) | 150 | 170 | 90 |
D’après INAO inao.gouv.fr ; fédération nationale Terra Vitis ; demeter.fr
Le dioxyde de soufre se trouve sous différentes formes dans le vin. On réalise donc un traitement du vin pour que tout ce dioxyde de soufre se retrouve sous forme (SO2,H2O(aq)) et on obtient alors la solution S2 qu’on titre.
Le titrage du dioxyde de soufre total contenu dans S2 est réalisé en milieu acide par la solution S1 de concentration connue en diiode égale à c1 = 5,0 × 10-4 mol·L-1.
L’indicateur de fin de réaction est l’empois d’amidon. Lorsque tout le (SO2,H2O(aq)) a réagi, le diiode forme un complexe bleu-noir avec l’empois d’amidon.
Protocole du titrage :
- prélever 10,0 mL de solution S2 et les verser dans un bécher ;
- on ajoute quelques gouttes d’empois d’amidon dans S2, celui-ci joue le rôle d’indicateur coloré de fin de réaction ;
- on titre à l’aide de la solution de diiode S1 de concentration c1 ;
- on observe un changement de couleur de l’empois d’amidon pour un volume de solution titrante versé Ve = 9,9 mL.
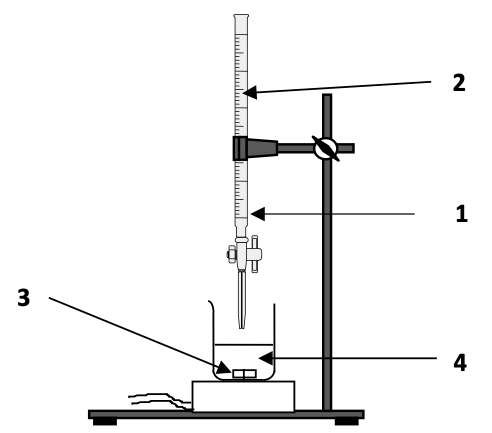
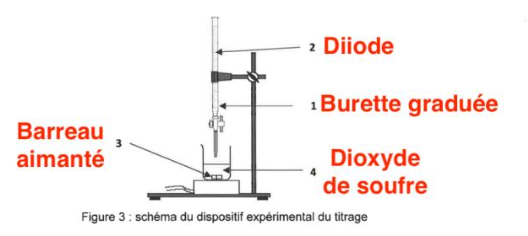
Figure 3 : schéma du dispositif expérimental du titrage
Q.13. Associer, sur votre copie, à chaque numéro (1, 2, 3, 4) du schéma du dispositif expérimental, un nom de matériel ou d’espèce chimique.
1 : Burette graduée
2 : Diiode
3 : Barreau aimanté
4 : Dioxyde de soufre
Q.14. Montrer que l’équation de la réaction support du titrage est :
H2SO3(aq) + I2(aq) + H2O(ℓ) → SO42-(aq) + 4 H+(aq) + 2 I–(aq)
$SO_4^{2-}\left(aq\right)/H_2SO_3\left(aq\right)$ :
$$H_2SO_3\left(aq\right)+H_2O\left(l\right)=SO_4^{2-}\left(aq\right)+4H^+\left(aq\right)+2e^-\left(aq\right)$$
$I_2\left(aq\right)/I^-\left(aq\right)$ :
$$I_2\left(aq\right)+2e^-\left(aq\right)=2I^-\left(aq\right)$$
$$H_2SO_3\left(aq\right)+H_2O\left(l\right)+I_2\left(aq\right)=SO_4^{2-}\left(aq\right)+4H^+\left(aq\right)+2I^-\left(aq\right)$$
Q.15. Établir la relation à l’équivalence entre les quantités de matière nE(I2(aq)) de diiode introduit et n0(H2SO3(aq)) de dioxyde de soufre dissous dans le vin.
$$H_2SO_3\left(aq\right)+H_2O\left(l\right)+I_2\left(aq\right)=SO_4^{2-}\left(aq\right)+4H^+\left(aq\right)+2I^-\left(aq\right)$$
À l’équivalence, les réactifs sont introduits dans les proportions stœchiométriques :
$$\frac{n_0\left(H_2SO_3\left(aq\right)\right)}{1}=\frac{n_E\left(I_2\left(aq\right)\right)}{1}$$
$$n_0\left(H_2SO_3\left(aq\right)\right)=n_E\left(I_2\left(aq\right)\right)$$
Q.16. Indiquer si le vigneron peut prétendre obtenir l’une ou l’autre de ces certifications.
Le candidat est invité à prendre des initiatives et à présenter la démarche suivie, même si elle n’a pas abouti. La démarche est évaluée et nécessite d’être correctement présentée.
$$n_0\left(H_2SO_3\left(aq\right)\right)=n_E\left(I_2\left(aq\right)\right)$$
$$C_2\times V_2=C_1\times V_e$$
$$C_2=\frac{C_1\times V_e}{V_2}$$
$$C_2=\frac{5,0\times 10^{-4}\times 9,9}{10,0}$$
$$C_2=5,0\times 10^{-4}\ mol.L^{-1}$$
Calculons la concentration massique :
$$C_m=C_2\times M$$
$$C_m=5,0\times 10^{-4}\times 82,1$$
$$C_m=4,1\times 10^{-2}\ g.L^{-1}$$
$$C_m=41\ mg.L^{-1}$$
Le taux de dioxyde de soufre total présent dans le vin pour différents labels doit être inférieur aux valeurs suivantes :
$150\ mg.L^{-1}$ pour la Certification AB
$170\ mg.L^{-1}$ pour la Certification Terra Vitis
$90\ mg.L^{-1}$ pour la Certification Demeter
Le taux de dioxyde de soufre total présent dans le vin est inférieur à toutes ces valeurs. Ainsi, le vigneron peut prétendre obtenir toutes les certifications (AB, Terra Vitis et Demeter).
