Bac Métropole Septembre 2021 Sujet 2
Exercice B – (5 points) – au choix du candidat – Durée 0h53 – Calculatrice autorisée
Sujet n° 21-PYCJ2ME3
Sujet et corrigé

Photographie de piles AA
de capacité 2800 mAh
Mots-clés : piles ; évolution d’un système
Chaque année en France, 1,3 milliard de piles sont vendues dans le commerce. Petits réservoirs d’énergie, elles constituent des objets indispensables au quotidien. L’objectif de cet exercice est d’étudier le fonctionnement d’une pile réalisée au laboratoire et de comparer sa capacité électrique à celle d’une pile AA vendue dans le commerce, photographiée ci-contre.
Données :
- masses molaires :
| espèce chimique | Aℓ | Aℓ2(SO4)3 |
| masse molaire en g·mol–1 | 27,0 | 342,15 |
Photographie de piles AA de capacité 2800 mAh
- couples oxydants-réducteurs : (Cu2+(aq) / Cu(s)) et (Aℓ3+(aq) / Aℓ(s)) ;
- charge élémentaire : e = 1,602×10–19 C ;
- constante d’Avogadro : NA = 6,022×1023 mol–1 ;
- 1 mAh = 3,60 C.
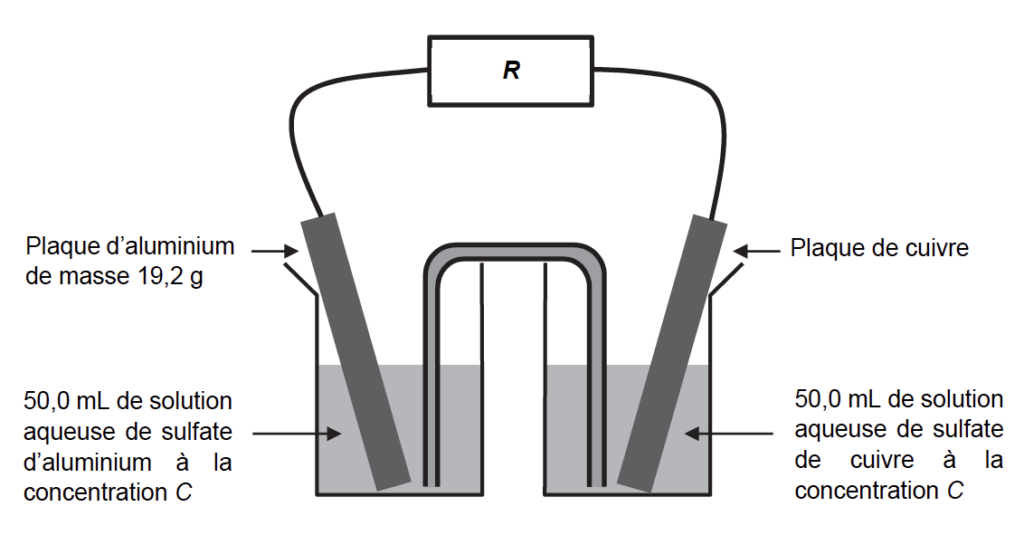
Pour réaliser la pile étudiée, deux solutions aqueuses sont préparées : une de sulfate d’aluminium notée S, et une de sulfate de cuivre (Cu2+(aq) ; SO42–(aq)), notée S’, toutes les deux sont à la concentration en soluté apporté de C = 0,100 mol·L-1. Le sulfate d’aluminium est un solide de formule Aℓ2(SO4)3(s), disponible sous forme de poudre.
1. Rédiger le protocole expérimental précis à mettre en œuvre pour préparer 50,0 mL de la solution S à partir du sulfate d’aluminium en poudre.
Calculons la masse à prélever :
$$n=\frac{m}{M}$$
$$m=n\times M$$
Or
$$c=\frac{n}{V}$$
$$n=c\times V$$
Ainsi
$$m=c\times V\times M$$
$$m=0,100\times50,0.{10}^{-3}\times342,15=1,71\ g$$
Protocole de dissolution :
- Peser précisément la masse $1,71\ g$ de sulfate d’aluminium solide dans une coupelle.
- Prendre une fiole jaugée de $50,0\ mL$ et introduire à l’aide d’un entonnoir la masse $m$ pesée.
- Remplir la fiole jaugée au ¾ avec de l’eau distillée.
- Boucher la fiole et agiter.
- Remplir la fiole jaugée jusqu’au trait de jauge avec de l’eau distillée.
- Boucher la fiole et agiter pour homogénéiser.
2. Calculer les concentrations en quantité de matière en ions aluminium Aℓ3+(aq) et en ion sulfate SO42–(aq) dans la solution S.
$${\rm Al}2({\rm SO}4){3(s)}\rightarrow2{\rm Al}{(aq)}^{3+}+3{\rm SO}_{4(aq)}^{2-}$$
Ainsi :
$$[{\rm Al}^{3+}]=2C=2\times0,100=0,200\ mol{.L}^{-1}$$
$$[{\rm SO}_4^{2-}]=3C=3\times0,100=0,300\ mol{.L}^{-1}$$
La pile est assemblée selon le schéma de la figure 1 représenté ci-dessous :
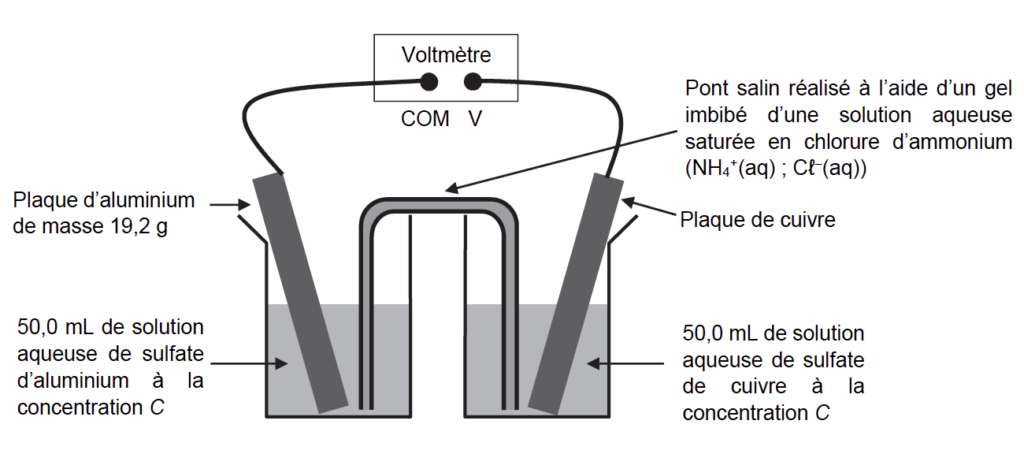
Pour déterminer la polarité de la pile ainsi constituée, un voltmètre est relié aux deux plaques métalliques. La borne COM du voltmètre est reliée à la plaque d’aluminium. Dans ces conditions, la tension mesurée aux bornes de la pile vaut U = 0,92 V.
3. Déterminer le pôle positif de la pile à l’aide du montage expérimental de la figure 1.
Le voltmètre fournit une valeur positive lorsque la borne « com » est reliée à la borne négative de la pile.
Ici le voltmètre donne une valeur positive, la borne « com » est donc reliée à la borne négative de la pile.
Ainsi la borne négative est l’électrode d’aluminium et la borne positive est l’électrode de cuivre.
Dans la suite de l’étude, le voltmètre est retiré puis est remplacé par un conducteur ohmique de résistance R.
4. Compléter le schéma fourni EN ANNEXE À RENDRE AVEC LA COPIE en y indiquant la polarité de la pile, le sens du courant électrique et le sens de circulation des porteurs de charge dans la pile et à l’extérieur de la pile lors de son fonctionnement.
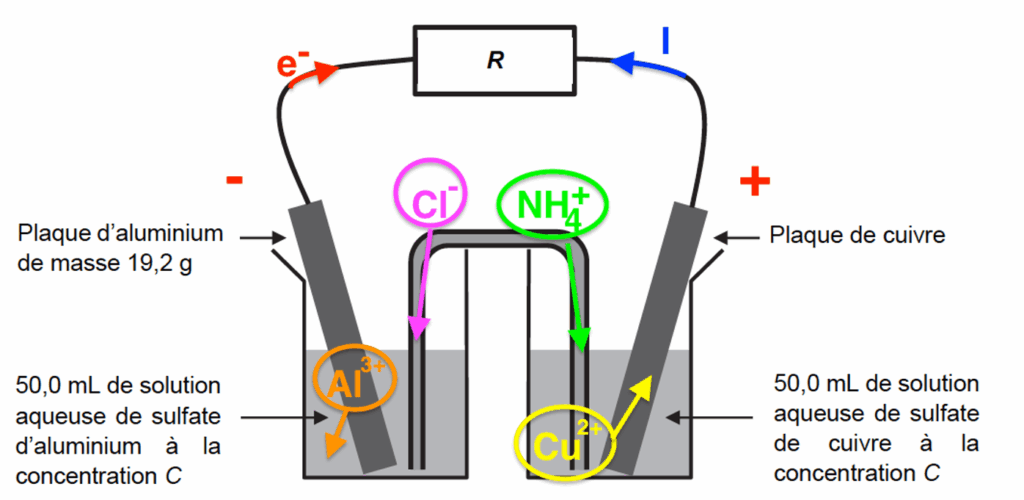
5. Établir les équations modélisant les réactions aux électrodes lors du fonctionnement de la pile. En déduire que l’équation de la réaction modélisant le fonctionnement de la pile s’écrit :
3Cu2+(aq) + 2Aℓ(s) ⇌ 3Cu(s) + 2Aℓ3+(aq)
La borne négative est la plaque d’aluminium, elle libère des électrons.
Les atomes d’aluminium se transforment donc en ions aluminium :
$${\rm Al}{(s)}={\rm Al}{(aq)}^{3+}+3e^-$$
La borne positive est la plaque de cuivre, elle consomme des électrons.
Les ions cuivre se transforment donc en atomes de cuivre :
$${\rm Cu}{(aq)}^{2+}+2e^-={\rm Cu}{(s)}$$
Soit :
$${\rm Al}{(s)}={\rm Al}{(aq)}^{3+}+3e^- \ \ \times2$$
$${\rm Cu}{(aq)}^{2+}+2e^-={\rm Cu}{(s)} \ \ \times3$$
L’équation de réaction est :
$$3{\rm Cu}{(aq)}^{2+}+2{\rm Al}{(s)}\rightleftarrows3{\rm Cu}{(s)}+2{\rm Al}{(aq)}^{3+}$$
La constante d’équilibre K associée à cette réaction a pour valeur K ≈ 10200, à 25 °C.
6. Montrer que la valeur initiale du quotient de réaction du système vaut Qr = 40. Conclure quant à l’évolution du système.
$$Q_{r,i}=\frac{[{\rm Al}^{3+}]_i^2}{[{\rm Cu}^{2+}]i^3}$$
$$Q{r,i}=\frac{(0,200)^2}{(0,100)^3}=40$$
$Q_{r,i}<K$ donc le sens d’évolution spontanée de la transformation est le sens direct.
7. Capacité électrique de la pile.
7.1. Déterminer quel est le réactif limitant.
$$x_{max1}=\frac{n_{{\rm Cu}^{2+}}^i}{3}=\frac{[{\rm Cu}^{2+}]\times V}{3}=\frac{0,100\times50,0.{10}^{-3}}{3}=1,67.{10}^{-3}\ mol$$
$$x_{max2}=\frac{n_{Al}^i}{2}=\frac{m_{Al}^i}{2\times M_{Al}}=\frac{19,2}{2\times27,0}=3,56.{10}^{-1}\ mol$$
$x_{max1}<x_{max2}$ donc les ions ${\rm Cu}^{2+}$ sont le réactif limitant.
7.2. Déterminer la capacité électrique Q de la pile du laboratoire, puis la comparer aux piles commerciales de type « AA ».
$$Q=n_{e^-}\times N_a\times e$$
Or d’après l’équation ${\rm Cu}{(aq)}^{2+}+2e^-={\rm Cu}{(s)}$
$$\frac{n_{e^-}}{2}=n_{{\rm Cu}^{2+}}^i$$
$$n_{e^-}=2\times n_{{\rm Cu}^{2+}}^i$$
$$n_{e^-}=2\times3\times x_{max1}$$
$$n_{e^-}=6\times x_{max1}$$
D’où :
$$Q=6\times x_{max1}\times N_a\times e$$
$$Q=6\times1,67.{10}^{-3}\times6,02.{10}^{23}\times1,602.{10}^{-19}$$
$$Q=966\ C$$
$$Q=\frac{966}{3,60}=268\ mAh$$
Comparaison :
$$\frac{Q_{AA}}{Q}=\frac{2800}{268}=10,4$$
Les piles commerciales de type « AA » ont des capacités 10 fois supérieures à celle de la pile du laboratoire.
8. Identifier un paramètre de la composition de la pile de laboratoire qu’il faudrait faire évoluer pour augmenter la capacité électrique de la pile, en précisant comment ce paramètre doit évoluer. Justifier.
$$Q=6\times x_{max1}\times N_a\times e$$
Pour augmenter Q, il faut augmenter $x_{max}$ ; ainsi, on peut augmenter la concentration en ions ${\rm Cu}^{2+}$.
ANNEXE À RENDRE AVEC LA COPIE