Bac Polynésie septembre 2023
Exercice 2 – (5 points) – Durée 0h53 – Calculatrice autorisée
Sujet n°23-PYCJ1PO3
Sujet et corrigé
EXERCICE 2 – L’ACIDE BUTANOÏQUE (5 points)
L’acide butanoïque de formule C3H7CO2H est présent dans le beurre rance, le fromage et dans le contenu gastrique. Il dégage une odeur forte et désagréable. Divers esters qui possèdent d’ailleurs des arômes plaisants sont obtenus à partir de l’acide butanoïque et sont utilisés dans l’industrie cosmétique pour des réactions d’estérification.
L’objectif de cet exercice est d’étudier l’influence de la concentration en quantité de matière d’acide butanoïque sur le quotient de réaction et de déterminer le taux d’avancement de la réaction.
Données :
- Couple acide-base de l’eau : H3O+(aq) / H2O(l)
- pKa du couple acide butanoique / ion butanoate à 25 °C : pKa = 4,82
- La conductivité σ d’une solution ionique peut s’exprimer en fonction de la concentration en quantité de matière [Xi] en ions dans la solution et des conductivités molaires ioniques λi de chaque ion Xi. (Loi de Kohlrausch)
$$ \sigma=\sum_i \lambda_i[X_i] $$
Avec σ en mS·m–1, λ en mS·m2·mol–1, [Xi] en mol·m–3
- λ(C3H7COO–) = 3,58 mS·m²·mol–1 et λ(H3O+) = 35,0 mS·m²·mol–1
- 1 mol·m–3 = 1 mmol·L–1
- Concentration en quantité de matière standard: C0 = 1 mol·L–1
Étude de l’influence de la concentration en acide butanoïque sur le quotient de réaction.
L’équation de la réaction modélisant la transformation entre l’acide butanoïque et l’eau est la suivante :
C3H7COOH(aq) + H2O(l) ⇄ C3H7COO–(aq) + H3O+(aq)
Q1. Identifier les couples acide/base mis en jeu dans cette transformation chimique.
$$C_3H_7COOH(aq)+H_2O(l)\rightleftarrows C_3H_7COO^-(aq)+H_3O^+(aq)$$
$C_3H_7COOH(aq)$ se transforme en $C_3H_7COO^-(aq)$ en perdant un proton $H^+$ selon la demi équation :
$$C_3H_7COOH(aq)=C_3H_7COO^-(aq)+H^+$$
Le couple acide/base correspondant est : $C_3H_7COOH(aq)/C_3H_7COO^-(aq)$
$H_2O(l)$ se transforme en $H_3O^+(aq)$ en gagnant un proton $H^+$ selon la demi équation :
$H_2O(l)+H^+=H_3O^+(aq)$
Le couple acide/base correspondant est : $H_3O^+(aq){/H}_2O(l)$
Q2. Compléter à l’aide d’expressions littérales le tableau d’avancement sur le document réponse à rendre obligatoirement avec la copie.
| C3H7COOH(aq) + H2O(l) ⇄ C3H7COO–(aq) + H3O+(aq) | |||||
| Avancement | Quantités de matière | ||||
| État initial | x = 0 | ni | excès | 0 | 0 |
| État intermédiaire | x | $$n_i-x$$ | excès | $$x$$ | $$x$$ |
| État final si réaction totale | x = xmax | $$n_i-x{max}$$ | excès | $$x_{max}$$ | $$x_{max}$$ |
| État final observé | x = xf | $$n_i-x_f$$ | excès | $$x_f$$ | $$x_f$$ |
Q3. En déduire la relation à l’état final entre [H3O+]f et [C3H7COO–]f.
$$\left[H_3O^+\right]_f=\frac{{n\left(H_3O^+\right)}_f}{V}$$
Or d’après le tableau d’avancement :
$${n\left(H_3O^+\right)}_f=x_f$$
$$\left[H_3O^+\right]_f=\frac{x_f}{V}$$
$$\left[C_3H_7COO^-\right]_f=\frac{{n\left(C_3H_7COO^-\right)}_f}{V}$$
Or d’après le tableau d’avancement :
$${n\left(C_3H_7COO^-\right)}_f=x_f$$
$$\left[C_3H_7COO^-\right]_f=\frac{x_f}{V}$$
Ainsi :
$$\left[H_3O^+\right]_f=\left[C_3H_7COO^-\right]_f$$
On réalise trois solutions aqueuses d’acide butanoïque de concentration en quantité de matière en soluté apporté 10,0 mmol·L–1, 5,00 mmol·L–1 et 1,00 mmol·L–1. La valeur du volume V de chacune des solutions est égale à 1,00 L.
On mesure les conductivités σf de chaque mélange à l’état final. Les résultats sont regroupés dans le tableau ci-après :
| Échantillon | 1 | 2 | 3 |
| c (mmol·L–1) | 10,0 | 5,00 | 1,00 |
| σf (mS·m–1) | 14,70 | 10,31 | 4,45 |
Q4. En utilisant la loi de Kohlrausch, exprimer la conductivité σf à l’état final du mélange 1 en fonction des concentrations en quantité de matière des ions [H3O+]f et [C3H7COO–]f.
Loi de Kohlrausch :
$$\sigma=\Sigma\lambda_i\left[X_i\right]$$
$$\sigma=\lambda_{H_3O^+}\left[H_3O^+\right]+\lambda_{C_3H_7COO^-}\left[C_3H_7COO^-\right]$$
Ainsi :
$$\sigma_f=\lambda_{H_3O^+}\left[H_3O^+\right]f+\lambda_{C_3H_7COO^-}\left[C_3H_7COO^-\right]_f$$
Q5. Pour le mélange 1, vérifier que la valeur de la concentration en quantité de matière des ions [H3O+]f et [C3H7COO–]f présents à l’état final est égale à 0,381 mmol·L–1.
$$\sigma_f=\lambda_{H_3O^+}\left[H_3O^+\right]f+\lambda_{C_3H_7COO^-}\left[C_3H_7COO^-\right]_f$$
Or (voir Q3.)
$$\left[H_3O^+\right]_f=\left[C_3H_7COO^-\right]_f$$
Ainsi :
$$\sigma_f=\lambda_{H_3O^+}\left[H_3O^+\right]f+\lambda_{C_3H_7COO^-}\left[H_3O^+\right]f$$
$$\sigma_f=\left(\lambda_{H_3O^+}+\lambda_{C_3H_7COO^-}\right)\times\left[H_3O^+\right]f$$
$$\left(\lambda_{H_3O^+}+\lambda_{C_3H_7COO^-}\right)\times\left[H_3O^+\right]f=\sigma_f$$
$$\left[H_3O^+\right]f=\frac{\sigma_f}{\left(\lambda_{H_3O^+}+\lambda_{C_3H_7COO^-}\right)}$$
$$\left[H_3O^+\right]_f=\frac{14,70}{35,0+3,58}$$
$$\left[H_3O^+\right]_f=0,381\ mmol.L^{-1}$$ Ainsi :
$$\left[C_3H_7COO^-\right]_f=0,381\ mmol.L^{-1}$$
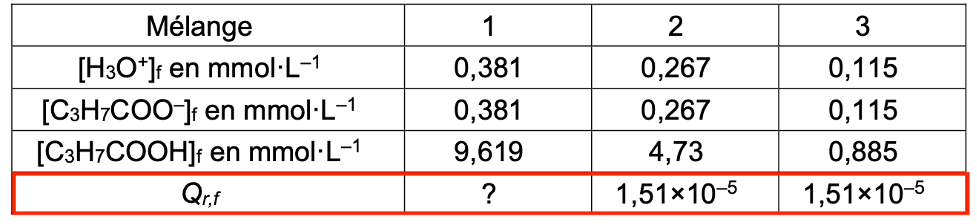
Le tableau ci-dessous regroupe les valeurs des concentrations en quantité de matière des espèces chimiques présentes dans les différents mélanges.
| Mélange | 1 | 2 | 3 |
| [H3O+]f en mmol·L–1 | 0,381 | 0,267 | 0,115 |
| [C3H7COO–]f en mmol·L–1 | 0,381 | 0,267 | 0,115 |
| [C3H7COOH]f en mmol·L–1 | 9,619 | 4,73 | 0,885 |
| Qr,f | ? | 1,51×10–5 | 1,51×10–5 |
Q6. Donner l’expression littérale du quotient de réaction Qr,f à l’état final en fonction des concentrations en quantité de matière [C3H7COOH]f, [H3O+]f, [C3H7COO–]f et C0 pour le mélange 1 puis calculer sa valeur. Commenter.
$$C_3H_7COOH(aq)+H_2O(l)\rightleftarrows C_3H_7COO^-(aq)+H_3O^+(aq)$$
$$Q_{r,f}=\frac{\left[H_3O^+\right]_f\times\left[C_3H_7COO^-\right]_f}{\left[C_3H_7COOH\right]_f\times C^0}$$
Pour le mélange 1 :
$$Q_{r,f}=\frac{0,381\times{10}^{-3}\times 0,381\times{10}^{-3}}{9,619\times{10}^{-3}\times 1}$$
$$Q_{r,f}=1,51\times{10}^{-5}$$
On remarque que la valeur de Qr,f est identique pour tous les mélanges.
Calcul du taux d’avancement de la réaction mettant en jeu la transformation de l’acide butanoïque avec l’eau dans le cas général.
On considère un volume V de valeur égale à 1,00 L d’une solution d’acide butanoïque de concentration en quantité de matière C de valeur égale à 1,0×10–3 mol·L–1 à 25 °C.
Q7. Établir que la constante d’équilibre Ka de la réaction mettant en jeu la transformation de l’acide butanoïque avec l’eau a pour expression :
$$ K_a=\frac{\left(\dfrac{x_f}{V}\right)^2}{\left(C-\dfrac{x_f}{V}\right)\times c^0}$$
On pourra s’aider du tableau d’avancement complété à la question Q2.
$$Ka=Q_{r,f}=\frac{\left[H_3O^+\right]_f\times\left[C_3H_7COO^-\right]_f}{\left[C_3H_7COOH\right]_f\times C^0}$$
| C3H7COOH(aq) + H2O(l) ⇄ C3H7COO–(aq) + H3O+(aq) | |||||
| Avancement | Quantités de matière | ||||
| État initial | x = 0 | ni | excès | 0 | 0 |
| État intermédiaire | x | $$n_i-x$$ | excès | $$x$$ | $$x$$ |
| État final si réaction totale | x = xmax | $$n_i-x{max}$$ | excès | $$x_{max}$$ | $$x_{max}$$ |
| État final observé | x = xf | $$n_i-x_f$$ | excès | $$x_f$$ | $$x_f$$ |
$$\left[H_3O^+\right]_f=\frac{{n\left(H_3O^+\right)}_f}{V}$$
Or d’après le tableau d’avancement :
$${n\left(H_3O^+\right)}_f=x_f$$
$$\left[H_3O^+\right]_f=\frac{x_f}{V}$$
$$\left[C_3H_7COO^-\right]_f=\frac{{n\left(C_3H_7COO^-\right)}_f}{V}$$
Or d’après le tableau d’avancement :
$${n\left(C_3H_7COO^-\right)}_f=x_f$$
$$\left[C_3H_7COO^-\right]_f=\frac{x_f}{V}$$
$$\left[C_3H_7COOH\right]_f=\frac{{n\left(C_3H_7COOH\right)}_f}{V}$$
Or d’après le tableau d’avancement :
$${n\left(C_3H_7COOH\right)}_f=n_i-x_f$$
$$\left[C_3H_7COOH\right]_f=\frac{n_i-x_f}{V}$$
Ainsi :
$$Ka=\frac{\frac{x_f}{V}\times\frac{x_f}{V}}{\frac{n_i-x_f}{V}\times C^0}$$
$$Ka=\frac{\left(\frac{x_f}{V}\right)^2}{\left(\frac{n_i}{V}-\frac{x_f}{V}\right)\times C^0}$$
Or
$$\frac{n_i}{V}=C$$
Ainsi :
$$Ka=\frac{\left(\frac{x_f}{V}\right)^2}{\left(C-\frac{x_f}{V}\right)\times C^0}$$
Q8. En déduire que, dans ce cas, le taux d’avancement de la réaction de l’acide butanoïque avec l’eau est proche de 12%.
$$Ka=\frac{\left(\frac{x_f}{V}\right)^2}{\left(C-\frac{x_f}{V}\right)\times C^0}$$
On remplace par les valeurs numériques :
$$K_A={10}^{-pKa}={10}^{-4,82}=1,51\times{10}^{-5}$$
$$C^0=1\ mol.L^{-1}$$
$$C=1,0\times{10}^{-3}\ mol.L^{-1}$$
$$V=1,00\ L$$
$$1,51\times{10}^{-5}=\frac{\left(\frac{x_f}{1,00}\right)^2}{\left(1,0\times{10}^{-3}-\frac{x_f}{1,00}\right)\times 1}$$
$$1,51\times{10}^{-5}=\frac{\left(x_f\right)^2}{\left(1,0\times{10}^{-3}-x_f\right)}$$
$$1,51\times{10}^{-5}\times\left(1,0\times{10}^{-3}-x_f\right)={x_f}^2$$
$$1,51\times{10}^{-5}\times 1,0\times{10}^{-3}-1,51\times{10}^{-5}\times x_f={x_f}^2$$
$$-{x_f}^2-1,51\times{10}^{-5}\times x_f+1,51\times{10}^{-8}=0$$
C’est une équation du second degré :
$$\Delta=b^2-4ac$$
$$\Delta=\left(-1,51\times{10}^{-5}\right)^2-4\times-1\times 1,51\times{10}^{-8}$$
$$\Delta=6,06\times{10}^{-8}$$
$${x_f}_1=\frac{-b+\sqrt\Delta}{2a}$$
$${x_f}_1=\frac{-\left(-1,51\times{10}^{-5}\right)+\sqrt{6,06\times{10}^{-8}}}{2\times-1}$$
$${x_f}_1=-1,31\times{10}^{-4}\ mol$$
$${x_f}_2=\frac{-b-\sqrt\Delta}{2a}$$
$${x_f}_2=\frac{-\left(-1,51\times{10}^{-5}\right)-\sqrt{6,06\times{10}^{-8}}}{2\times-1}$$
$${x_f}_2=1,16\times{10}^{-4}\ mol$$
On ne garde pas la valeur négative.
$$x_f=1,16\times{10}^{-4}\ mol$$
Trouvons $x_{max}$ :
$$n_i-x_{max}=0$$
$$-x_{max}=-n_i$$
$$x_{max}=n_i$$
$$x_{max}=C\times V$$
$$x_{max}=1,0\times{10}^{-3}\times 1,00$$
$$x_{max}=1,0\times{10}^{-3}\ mol$$
Calculons le taux d’avancement de la réaction de l’acide butanoïque avec l’eau :
$$\tau=\frac{x_f}{x_{max}}$$
$$\tau=\frac{1,16\times{10}^{-4}}{1,0\times{10}^{-3}}$$
$$\tau=0,12$$
$$\tau=12%$$
DOCUMENT RÉPONSE À RENDRE OBLIGATOIREMENT AVEC LA COPIE
EXERCICE 2 – L’ACIDE BUTANOÏQUE
Q2. Compléter le tableau d’avancement
| C3H7COOH(aq) + H2O(l) ⇄ C3H7COO–(aq) + H3O+(aq) | |||||
| Avancement | Quantités de matière | ||||
| État initial | x = 0 | ni | excès | ||
| État intermédiaire | x | excès | |||
| État final si réaction totale | x = xmax | excès | |||
| État final observé | x = xf | excès | |||
