Métropole Septembre 2022 Sujet 2
Exercice A – (5 points) – au choix du candidat – Durée 0h53 – Calculatrice autorisée
Sujet n° 22-PYCJ2ME3
Sujet et corrigé
Mots-clés : synthèse organique
L’acide benzoïque, connu dans l’alimentation sous la dénomination E210, est aussi utilisé en tant que conservateur dans les cosmétiques. Cette molécule qui empêche le développement de bactéries est également autorisée dans les cosmétiques bio.
L’objectif de l’exercice est d’étudier les étapes de la synthèse de l’acide benzoïque en utilisant la réaction de Cannizzaro.
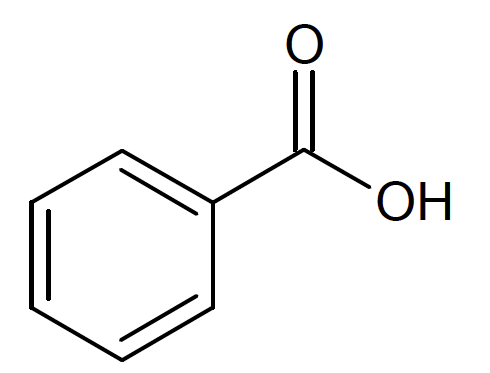
Figure 1. Formule topologique de l’acide benzoïque
Données :
| Espèce chimique | Masse molaire en g∙mol–1 | Densité | Solubilité dans l’eau | Solubilité dans l’éther diéthylique | Température de fusion en °C |
| Benzaldéhyde C7H6O | 106 | 1,05 | Très faible | Très grande | – 26 |
| Acide benzoïque C7H6O2 | 122 | Très faible | Faible | 122,3 | |
| Ion benzoate C7H5O2− | 121 | Très élevée | Très faible | ||
| Alcool benzylique C7H8O | 108 | 1,04 | Faible | Très grande | – 15 |
| Hydroxyde de potassium KOH | 56 | Très grande | Très faible | 360 | |
| Eau H2O | 18 | 1,0 | Insoluble | 0 | |
| Ether diéthylique C4H10O | 74 | 0,71 | Insoluble | – 116,3 |
- pKA à 25°C du couple acide benzoïque C7H6O2(aq) / ion benzoate C7H5O− (aq) : 4,2.
La synthèse de l’acide benzoïque à partir du benzaldéhyde met en jeu successivement deux transformations chimiques modélisées par les réactions d’équations indiquées ci-dessous.
La réaction n°1, nommée réaction de Cannizzaro, a lieu en milieu très basique. Elle fait intervenir deux molécules de benzaldéhyde, l’une jouant le rôle d’oxydant et l’autre de réducteur.
- Réaction n°1 (réaction de Cannizzaro) :
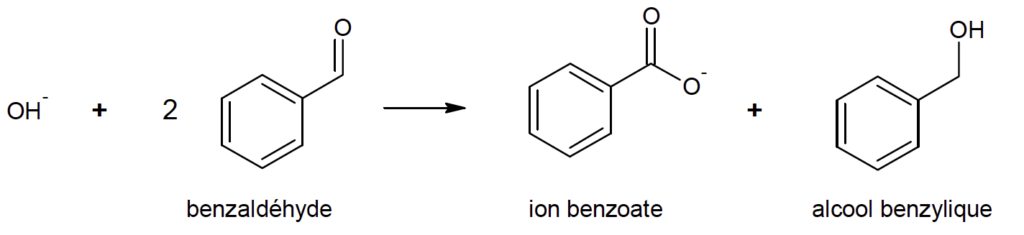
- Réaction n°2 :
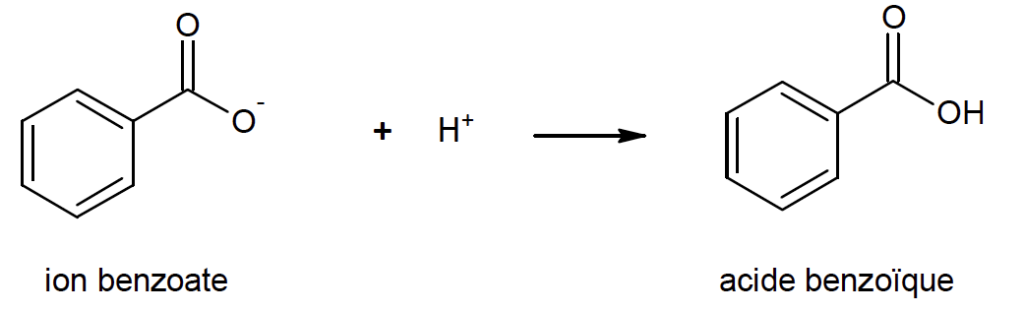
1. Étude de la réaction n°1 (réaction de Cannizzaro)
Q1. Représenter la formule semi-développée de l’acide benzoïque, entourer le groupe caractéristique et identifier la famille fonctionnelle correspondante.
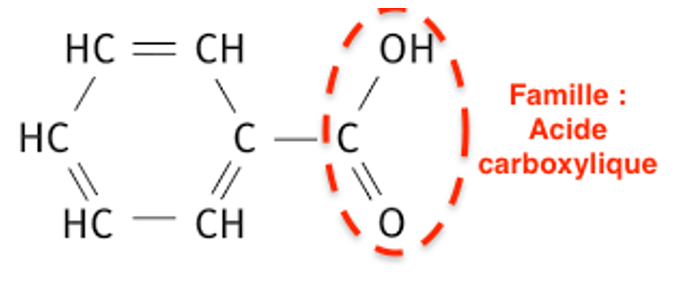
Q2. Justifier, à l’aide d’un diagramme de prédominance, l’obtention de l’ion benzoate lors de transformation chimique modélisée par la réaction n°1.
Diagramme de prédominance :
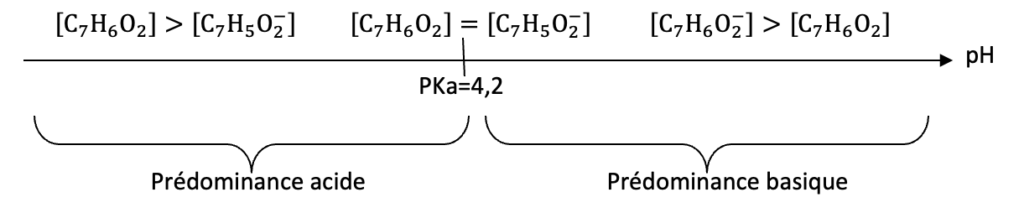
D’après l’énoncé : « la réaction n°1 a lieu en milieu très basique ». Le pH du milieu est donc supérieur à 7.
D’après le diagramme de prédominance ${{C_7H}_5O}_2^-$, l’ion benzoate, est prédominant.
Q3. Écrire la demi-équation électronique modélisant le transfert d’électrons entre le benzaldéhyde C7H6O(aq) et l’alcool benzylique C7H8O(aq), et identifier l’espèce oxydante et l’espèce réductrice du couple associé.
${C_7H}_6O_{(aq)}+2H^++2e^-={C_7H}_8O_{(aq)}$
${C_7H}_6O_{(aq)}$ est capable de capter des électrons : c’est un oxydant.
${C_7H}_8O_{(aq)}$ est capable de céder des électrons : c’est un réducteur.
2. Étude du protocole expérimental
On donne ci-dessous un protocole expérimental permettant d’obtenir l’acide benzoïque par la réaction de Cannizzaro.
①
a) Dans un erlenmeyer, dissoudre une masse de 10 g d’hydroxyde de potassium dans 40 mL d’eau distillée.
b) Ajouter 5,0 mL de benzaldéhyde. Agiter vigoureusement, puis laisser sous agitation à température ambiante pendant 48 h.
②
c) Ajouter 20 mL d’éther diéthylique dans le milieu réactionnel, agiter, puis transvaser dans une ampoule à décanter.
d) Séparer la phase aqueuse de la phase organique.
e) Récupérer la phase aqueuse dans un erlenmeyer et la placer dans un bain d’eau glacée.
③
f) Sous la hotte, ajouter lentement dans la phase aqueuse, en agitant, une solution d’acide chlorhydrique jusqu’à pH = 2 : un solide blanc précipite.
④
g) Filtrer sur Büchner.
⑤
h) Introduire le produit obtenu dans un bécher avec 10 mL d’eau. Chauffer et ajouter la quantité d’eau juste nécessaire pour dissoudre le produit.
i) Laisser refroidir lentement puis filtrer sur un entonnoir Büchner pour récupérer le produit recristallisé.
j) Placer le produit à l’étuve puis peser le produit sec.
⑥
k) Réaliser la chromatographie sur couche mince du produit obtenu.
On obtient une masse m = 1,1 g de produit synthétisé.
On donne sur la figure 2 le résultat de la chromatographie sur couche mince (CCM) obtenue.
Les produits déposés sont en solution dans de l’éther diéthylique.
Dépôt A : benzaldéhyde commercial Dépôt B : acide benzoïque commercial Dépôt C : produit synthétisé.
La révélation se fait sous lampe UV.

Q4. Pour chaque étape du protocole numérotée de ① à ⑥ indiquer, sans justifier, si cette étape correspond à une transformation chimique de réactifs, à une analyse du produit synthétisé, à une purification ou à une séparation.
| 1 | Transformation chimique de réactifs |
| 2 | Séparation |
| 3 | Séparation |
| 4 | Séparation |
| 5 | Purification |
| 6 | Analyse du produit synthétisé |
Q5. Proposer, en justifiant, un dispositif expérimental permettant d’optimiser la vitesse de formation du produit de synthèse.
La température est un facteur cinétique.
Lorsque la température augmente, la vitesse de formation du produit augmente.
On pourrait utiliser le chauffage à reflux qui accélère la réaction sans perte de matière.
Q6. Schématiser l’ampoule à décanter et son contenu en justifiant la position relative des deux phases. Indiquer, en justifiant, les phases dans lesquelles se situent l’ion benzoate et l’alcool benzylique produits lors de l’étape 1.
| Phase aqueuse | Phase organique |
| eau | éther diéthylique |
$d_{eau}=1{,}0$ et $d_{\text{éther diéthylique}}=0{,}71$
$d_{eau}>d_{\text{éther diéthylique}}$
La densité de l’eau est supérieure à celle de l’éther diéthylique : la phase aqueuse est en bas et la phase organique en haut.
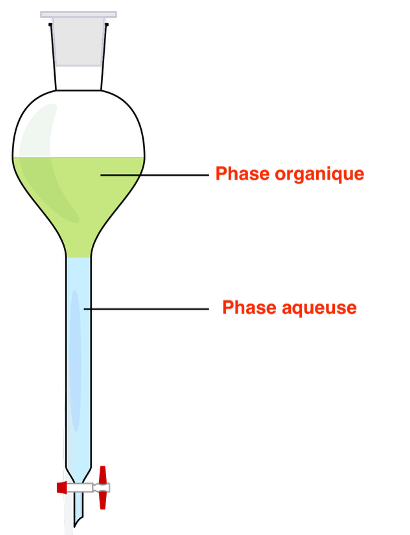
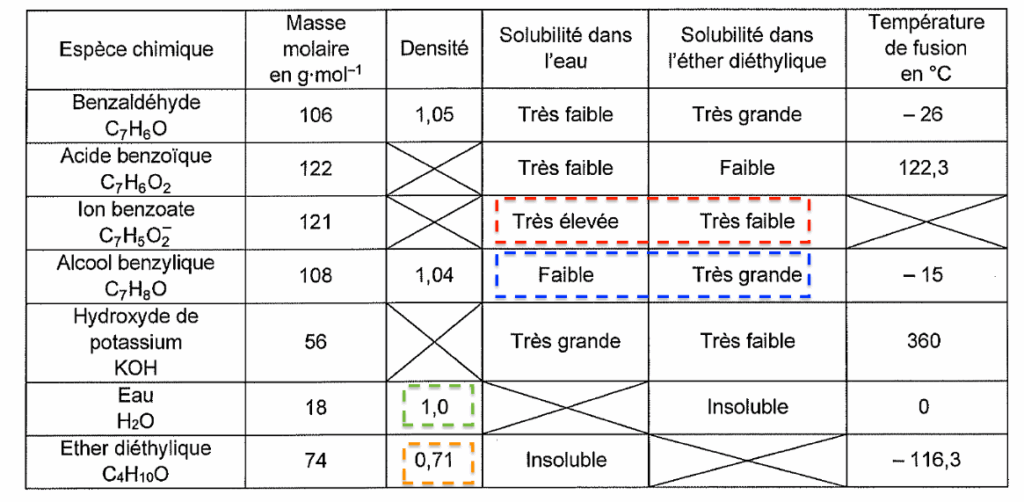
- ion benzoate : solubilité dans l’eau très élevée et dans l’éther diéthylique très faible. L’ion benzoate est donc dans la phase aqueuse.
- Alcool benzylique: solubilité dans l’eau faible et dans l’éther diéthylique très grande. L’alcool benzylique est donc dans la phase organique.
Q7. À l’étape f du protocole expérimental, justifier à l’aide des données l’apparition d’un solide.
Lors de l’étape f nous ajoutons de l’acide chlorhydrique à la phase aqueuse qui contient l’ion benzoate (question 6).
Le pH de la solution diminue jusqu’a pH=2.
D’après le diagramme de prédominance (question 2), pour pH=2 l’acide benzoïque est prédominant car le pH<pKa.
Ainsi, l’ion benzoate se transforme en acide benzoïque lors de l’ajout d’acide chlorhydrique.
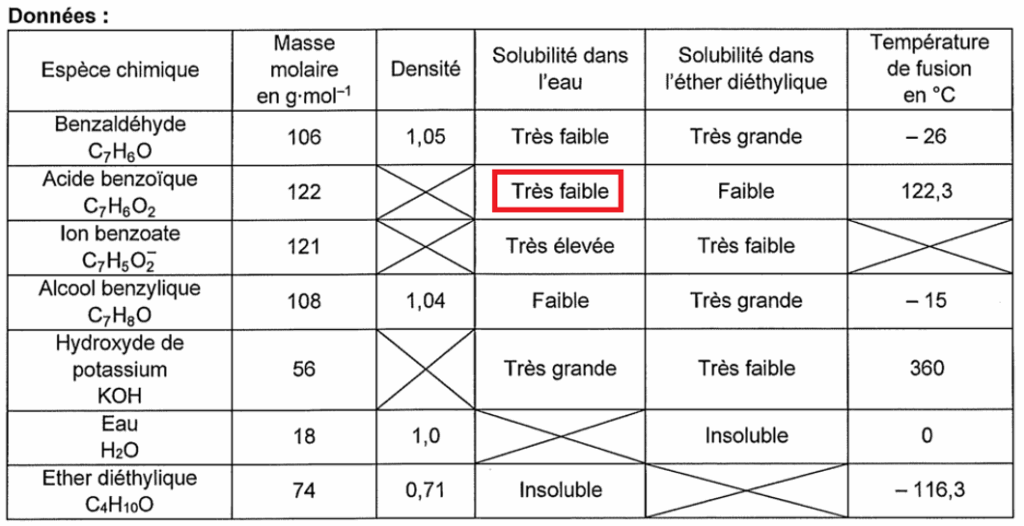
Or l’acide benzoïque n’est que très faiblement soluble dans l’eau : un solide apparait.
Q8. Interpréter le résultat de la chromatographie sur couche mince obtenu.
Le dépôt C correspond au produit synthétisé.
Sur le chromatogramme nous observons une seule tache : le produit synthétisé est pur.
Sur le chromatogramme nous observons que la tache du produit C est au même niveau que celle du produit B. Le produit synthétisé est donc identique au produit B : le produit C est de l’acide benzoïque.

Q9. Déterminer la valeur du rendement de la synthèse de l’acide benzoïque. Commenter.
Réaction n°1 : ${\rm HO}_{(aq)}^-+2{C_7H}_6O_{(aq)}\rightarrow{{C_7H}_6O}_{2(aq)}^-+{C_7H}_8O_{(aq)}$
Réaction n°2 : ${{C_7H}_6O}_{2(aq)}^-+H_{(aq)}^+\rightarrow{C_7H}_8O_{2(aq)}$
Bilan :
${\rm HO}_{(aq)}^-+2{C_7H}_6O_{(aq)}+{{C_7H}_6O}_{2(aq)}^-+H_{(aq)}^+\rightarrow{{C_7H}_6O}_{2(aq)}^-+{C_7H}_8O_{(aq)}+{C_7H}_8O_{2(aq)}$
${\rm HO}_{(aq)}^-+2{C_7H}_6O_{(aq)}+H_{(aq)}^+\rightarrow{C_7H}_8O_{(aq)}+{C_7H}_8O_{2(aq)}$
Quantités de matière des réactifs :
$n_{{\rm HO}^-}=n_{\text{Hydroxyde de potassium}}=\dfrac{m_{\text{Hydroxyde de potassium}}}{M_{\text{Hydroxyde de potassium}}}$
$n_{{\rm HO}^-}=\dfrac{10}{56}$
$n_{{\rm HO}^-}=0{,}18\ \text{mol}$
$n_{\text{benzaldéhyde}}=\dfrac{m_{\text{benzaldéhyde}}}{M_{\text{benzaldéhyde}}}$
Or $\rho_{\text{benzaldéhyde}}=\dfrac{m_{\text{benzaldéhyde}}}{V_{\text{benzaldéhyde}}}$ donc $m_{\text{benzaldéhyde}}=\rho_{\text{benzaldéhyde}} \times V_{\text{benzaldéhyde}}$
$n_{\text{benzaldéhyde}}=\dfrac{\rho_{\text{benzaldéhyde}} \times V_{\text{benzaldéhyde}}}{M_{\text{benzaldéhyde}}}$
Or $d_{\text{benzaldéhyde}}=\dfrac{\rho_{\text{benzaldéhyde}}}{\rho_{eau}}$
$\rho_{\text{benzaldéhyde}}=d_{\text{benzaldéhyde}} \times \rho_{eau}$
$n_{\text{benzaldéhyde}}=\dfrac{d_{\text{benzaldéhyde}} \times \rho_{eau} \times V_{\text{benzaldéhyde}}}{M_{\text{benzaldéhyde}}}$
$n_{\text{benzaldéhyde}}=\dfrac{1{,}05 \times 1000 \times 5{,}0 \times {10}^{-3}}{106}=5{,}0 \times {10}^{-2}\ \text{mol}$
| $HO^-$ | $+2C_7H_6O $ | $ H^+$ | $\rightarrow C_7H_8O$ | $+ C_7H_8O_2$ | |
| Etat initial | 0,18 | 5,0×10-2 | Excès | 0 | 0 |
| Etat intermédiaire | 0,18-x | 5,0×10-2-x | Excès | x | x |
| Etat final | 0,18-xf | 5,0×10-2-xf | Excès | xf | xf |
Calculons l’avancement maximal :
$0{,}18-x_{max1}=0 \ \Rightarrow\ x_{max1}=0{,}18\ \text{mol}$
$5{,}0{\times }{10}^{-2}-2x_{max2}=0 \ \Rightarrow\ x_{max2}=\dfrac{5{,}0{\times }{10}^{-2}}{2}=2{,}5{\times }{10}^{-2}\ \text{mol}$
$x_{max2}<x_{max1}$
Donc $x_{max}=x_{max2}$ , le benzaldéhyde est le réactif limitant
Calculons la masse théorique d’acide benzoïque que l’on pourrait obtenir si la synthèse était totale :
$m_{\text{acide benzoïque}}^{\text{théorique}}=n_{\text{acide benzoïque}} \times M_{\text{acide benzoïque}}$
$m_{\text{acide benzoïque}}=x_{max} \times M_{\text{acide benzoïque}}$
$m_{\text{acide benzoïque}}=2{,}5 \times {10}^{-2} \times 122$
$m_{\text{acide benzoïque}}=3{,}1\ \text{g}$
Calculons le rendement :
$\eta=\dfrac{m_{\text{exp}}}{m_{\text{acide benzoïque}}^{\text{théorique}}}$
$\eta=\dfrac{1{,}1}{3{,}1}$
$\eta=0{,}35=35%$
La réaction n’est pas totale.
