Bac Métropole Mars 2021 Sujet 1
Exercice A – (5 points) – au choix du candidat – Durée 0h53 – Calculatrice autorisée
Sujet et corrigé
Mots-clés : réactions acide-base ; dosage par titrage
Les anthocyanes sont des espèces chimiques responsables de la couleur de nombreux végétaux comme le chou rouge, l’hortensia ou encore l’aubergine. Une des propriétés remarquables des anthocyanes est que leur couleur en solution dépend fortement du pH de la solution.
Dans cet exercice, on se propose de modéliser un indicateur coloré naturel contenant des anthocyanes pour pouvoir l’utiliser lors du titrage d’un lait fermenté.
Données :
- numéros atomiques des éléments hydrogène, carbone et oxygène :
| Élément chimique | H | C | O |
| Numéro atomique | 1 | 6 | 8 |
- constante d’acidité à 20°C du couple acide lactique / ion lactate : KA = 10–3,9 ;
- masse molaire de l’acide lactique : MAH = 90,1 g⋅mol–1 ;
- l’acidité Dornic d’un lait, exprimée en degré Dornic de symbole °D, est reliée à la concentration en masse d’acide lactique dans ce lait en considérant qu’il est le seul acide présent : 1,0 °D correspond à une concentration en masse en acide lactique égale à 0,10 g·L–1.
1. Modélisation d’un indicateur coloré naturel issu du chou rouge
La couleur du chou rouge est principalement due à la présence d’une vingtaine d’anthocyanes différentes. Pour comprendre l’influence du pH du milieu sur la couleur, on modélise ce mélange complexe d’espèces chimiques par une seule espèce chimique, la cyanidine (figure 1), dont la structure est commune à toutes les anthocyanes.
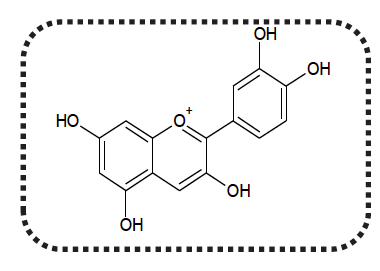
On limite la modélisation à des milieux où le pH est compris entre 4,5 et 9,0. Dans cet intervalle, la cyanidine existe principalement sous trois formes :
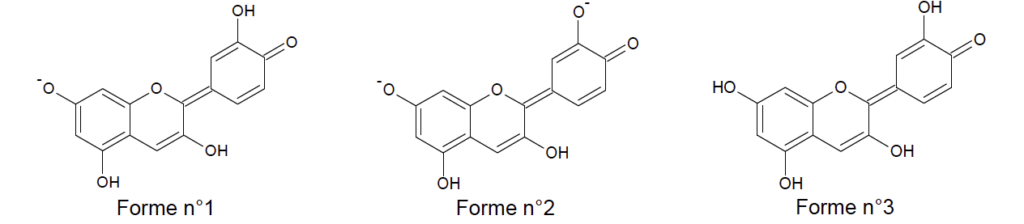
Au laboratoire, on prépare une solution de jus de chou rouge en faisant macérer pendant dix minutes dans de l’eau distillée chaude le quart d’un chou rouge coupé en morceaux. On filtre le mélange et on obtient une solution aqueuse de couleur violet-bleu intense. On fait varier le pH de la solution et on note la couleur correspondante :
| Couleur | Violet | Violet | Violet- bleu | Violet- bleu | Bleu | Bleu | Bleu- Vert | Bleu- Vert | Vert | Vert |
| pH | 4,5 | 5,0 | 5,5 | 6,0 | 6,5 | 7,0 | 7,5 | 8,0 | 8,5 | 9,0 |
1.1. Justifier que la forme n°1 est une espèce amphotère.
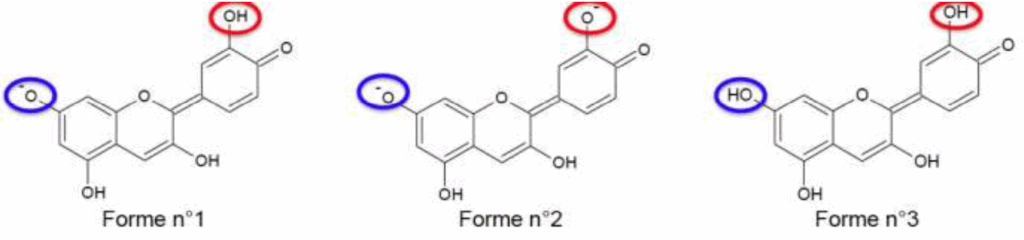
La forme 1 passe à la forme 2 en cédant un H+. On à donc le couple Forme n°1/ Forme n°2
La forme 3 passe à la forme 1 en cédant un H+. On à donc le couple Forme n°3/ Forme n°1
La Forme n°1 est donc à la fois un acide et une base : c’est une espèce amphotère.
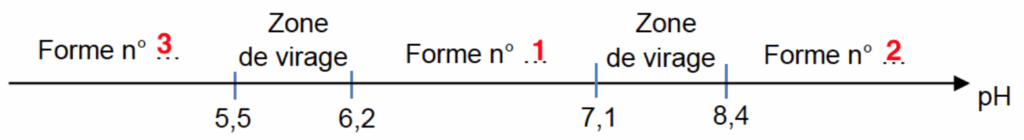
1.2. Recopier puis compléter les pointillés du diagramme de prédominance ci-après pour cet indicateur coloré. Associer une couleur à chaque forme en solution aqueuse.
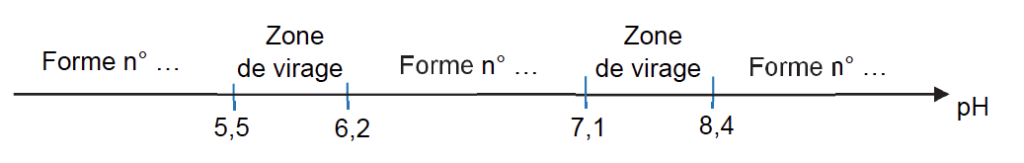
2. Titrage d’un lait fermenté
Pour préparer des fromages ou des yaourts, il est nécessaire de faire fermenter du lait frais. Des bactéries appelées ferments lactiques sont utilisées pour transformer notamment le lactose du lait frais en acide lactique (figure 2).
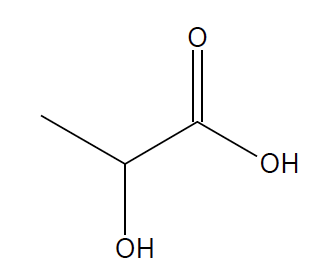
Figure 2. Formule topologique
de l’acide lactique
Lors de la fabrication des produits laitiers, pour déterminer l’avancement de la fermentation du lait, les techniciens réalisent un titrage acido- basique de l’acide lactique formé afin de déterminer l’acidité Dornic.
L’acidité Dornic d’un lait doit être supérieure à 80 °D pour pouvoir fabriquer un yaourt.
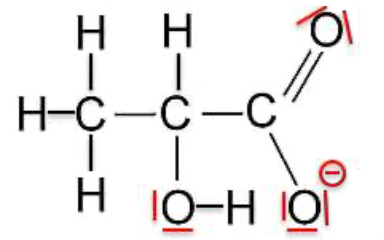
2.1. Représenter le schéma de Lewis de l’ion lactate.
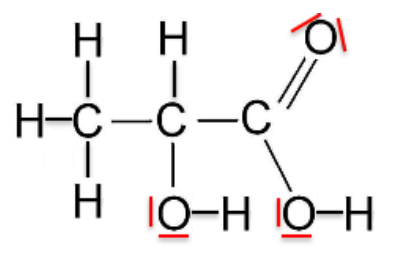
Acide lactique :
Ion lactate :
2.2. Justifier que la fermentation du lait contribue à acidifier celui-ci.
« … fermenter du lait frais. Des bactéries appelées ferments lactiques sont utilisées pour transformer notamment le lactose du lait frais en acide lactique »
Il se forme donc de l’acide AH lors de la fermentation du lait : le lait s’acidifie.
2.3. On veut modéliser la transformation chimique entre l’acide lactique et l’eau du lait. On notera AH l’acide lactique et A– l’ion lactate.
2.3.1. Écrire l’équation de la réaction modélisant cette transformation chimique.
$$HA_{(aq)}+H_2O_{(l)} \rightleftarrows A_{(aq)}^-+\ H_3O_{(aq)}^+$$
2.3.2. Montrer que cette transformation chimique est spontanée. On admettra que la concentration initiale en ion lactate est nulle.
$$Q_{ri} = \frac{[A^-]_i \times [\text{H}_3\text{O}^+]_i}{[HA]_i \times c^0}$$
Or [A–]i=0, donc $Q_{ri}=0$
Ainsi $Q_{ri}$<$K_A$ , la transformation spontanée s’effectue dans le sens direct.
La méthode Dornic consiste à titrer 10,0 mL de lait par une solution aqueuse d’hydroxyde de sodium de concentration en quantité de matière C0 = 1,11×10–1 mol·L–1. On note VE le volume de solution titrante versée à l’équivalence.
On modélise la transformation chimique mise en jeu lors de ce titrage par une réaction support dont l’équation est la suivante :
AH(aq) + HO–(aq) → A–(aq) + H2O(ℓ)
On applique la méthode Dornic à un lait en utilisant le chou rouge comme indicateur coloré. Le pH initial vaut 5,9 et le pH à l’équivalence vaut 8,3. Le volume versé à l’équivalence est égal à 2,8 mL.
2.4. Justifier que le jus de chou rouge peut être utilisé pour repérer l’équivalence de ce titrage et préciser le changement de couleur du milieu.
« Le pH initial vaut 5,9 et le pH à l’équivalence vaut 8,3. »
Le pH à l’équivalence est compris dans la zone de virage. Ainsi le chou rouge peut être utilisé pour repérer l’équivalence de ce titrage.
Pour un pH de 5,9 la couleur est violet bleu et pour pH=8,3 la couleur est vert. Il y a donc un changement de couleur du violet-bleu au vert.
2.5. En détaillant le raisonnement, déterminer si l’acidité Dornic du lait fermenté testé permet la fabrication d’un yaourt.
Le candidat est invité à prendre des initiatives et à présenter la démarche suivie, même si elle n’a pas abouti. La démarche est évaluée et nécessite d’être correctement présentée.
A l’équivalence :
$$\frac{n_{AH}^i}{1}=\frac{n_{{\rm HO}^-}^{eq}}{1}$$
$$\frac{m_{AH}}{M_{AH}}=C_0 \times V_{eq}$$
$$m_{AH}=C_0 \times V_{eq} \times M_{AH}$$
$$m_{AH}=1,11 \times {10}^{-1} \times 2,8 \times {10}^{-3} \times 90,1$$
$$m_{AH}=2,8 \times {10}^{-2}g\ dans\ les\ 10\ mL$$
« l’acidité Dornic d’un lait, exprimée en degré Dornic de symbole °D, est reliée à la concentration en masse d’acide lactique dans ce lait en considérant qu’il est le seul acide présent »
Calculons sa concentration massique :
$$C_{m_{AH}}=\frac{m_{AH}}{V}$$
$$C_{m_{AH}}=\frac{2,8 \times {10}^{-2}}{10,0 \times {10}^{-3}}$$
$$C_{m_{AH}}=2,8\ g.L^{-1}$$
«1,0 °D correspond à une concentration en masse en acide lactique égale à 0,10 g·L–1»
Le lait a donc une acidité Dornic de 28°D.
Cette acidité est inférieure à 80°D, elle ne permet pas la fabrication d’un yaourt.
